��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��18�֣�����һ������ɫ���������Ľ���, 2000��ǰ������ѿ�ʼʹ������������Ϊ�����ڰ𣬻ƽ�������ĵ����ֹ�����������й�����������������ɫ�����кܺõ�ɱ��������������Ч�á������г�����ʳƷ���ʡ���ͷ�ڲ�ķ���Ĥ�ȡ���ش������й��������⣺
��1��������Ȼ�缸��������ʯ����ʽ���ڣ�����м��������������������ʯ��SnO2��Ϊԭ�ϣ��������Ľ�̿����ԭ�����ڸ����¿��Ƶô������÷�Ӧ�Ļ�ѧ����ʽΪ?????????????????����������⾫���ɵô���������ʱ��������ӦʽΪ____________��
��2�������Ȼ�����SnCl2��SnCl4��SnCl2�������ͻ�ѧʵ���г��õĻ�ԭ��������ˮ�⣻SnCl4����������ɫҺ�壬�ڿ����м���ˮ�⣬�۵㡪36�棬�е�114�档
����ʵ��������SnCl2��������SnCl2��Һ���Լ�����������?????��
��ijʵ��С����������ͼ�е������������װһ��ʵ��װ�ã������ڵĽ���������������ֱ��������ȡ��ˮ���Ȼ���(�˷�Ӧ���̷ų���������)����֪���������۵�Ϊ231�档��ش����и�����:
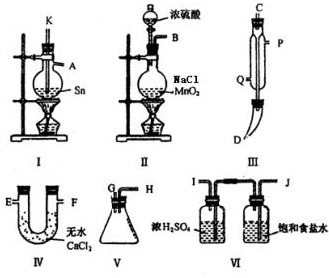
���ò���(δ����)��������װ�ã���ȷ��˳����(����ӿڵĴ�����ĸ)____��____��____��____��____��____��____��____��____��____��
��װ�â���������___________��װ�â���������___________��
������������ȴˮ�������Ǵ�___________���룬��___________������
������ʱ��ȼ�ƾ��ƣ������¶�Ӧ����?????????�棬��???????????????????����ֹͣ���ȡ�
���������ȡ�����Ȼ���������¶�ڿ����У�Ԥ�ڿɿ�����������_______________��
��ʵ��װ���л����ڵ�һ��������?????????????????????????????????��
�ο��𰸣���1��SnO2+C ��������������ͼӦ���ǣ�
��������������ͼӦ���ǣ�

��1����̿����ʯ�ڸ����·���������ԭ��Ӧ��������̿������ΪCO��������̼�ĵͼ��������ȶ���������SnO2+C Sn+CO
Sn+CO
�����ľ���ʱ����������������Һ�е������ӵõ���������Sn2++2e-="Sn"
��2�����ۺ���Ŀ������Ϣ��SnCl2��ˮ�⡢����������Ӧ��SnCl2�����ܽ�������Ũ�����У�������ˮ�⣬��ˮϡ�ͺӽ��������Է�ֹ��������Sn4++Sn=2Sn2+
����ȡ���Ȼ������ȵ���ȡ���﴿��������������װ��ΪII��VI���ñ���ʳ��ˮ����HCl���壬��Ũ������������ѭ�������̳������ӿ�˳��ΪB��J��I
װ��IΪ���Ȼ�������ȡװ�ã����ڷ�Ӧ�Ŵ������ȣ����������������������Ȼ�����ϴ��˹�A���ݳ��������Ҫ�����ܣ�װ��III��������ȴ�������������Ȼ���Һ���ռ�Ҫװ��V�У��ӿ�˳��ΪI��K��A��C��D��G��H
Ϊ��ֹ�����е�ˮ��������װ��V�У����Ȼ�������ˮ�⣬��֤����ˮ��������H�ӿں�Ӧ����װ��IV�����е�CaCl2����ֹ������ˮ�֣�
�ۺϿ�֪���ӿ�˳��ΪB��J��I��K��A��C��D��G��H��E
��װ�â��������dz�ȥCl2�е�HCl��ˮ����װ�â��������Ƿ�ֹ������ˮ���������ռ�SnCl4ƿ�ڣ�
��Ϊ��֤����ˮ������Ч����Ӧ�ӵͿ�Q�����߿�P����ʹ����������һֱ����ˮ
�ܼ����¶�ֻ�賬�����������۵�Ϊ231�漴�ɣ����ڷ�Ӧ�������ȣ��������ۻ���ֹͣ����
�����Ȼ���������¶�ڿ�������ˮˮ�⣬���ɴ����ļ�������ˮ��HCl���壬�γɰ���
�����������ж�������ʵ��ȱ��β������װ�ã�Ӧ��ʢ��NaOH������Һ���ձ����ն���Cl2
�����Ѷȣ�һ��
2��ʵ���� ( 14��)
(1)���������ڵ�����Ϊ���ʣ�����ȥ���и�������������������Լ���д�ں����ϣ�
��(�ױ�)????????����(�Ҵ�)????????���ױ�(��)????????��
��2��ʵ�����ɵ�ʯ�е�̼���ƺ�ˮ��Ӧ��ȡ��Ȳ���÷�Ӧ�Ļ�ѧ����ʽ Ϊ?????��ʵ����Ϊ�˼�����Ӧ���ʣ�����??????����ˮ����ʵ���в���������������ŵ���ζ��������_________________�����Լ������Գ�ȥ��
Ϊ?????��ʵ����Ϊ�˼�����Ӧ���ʣ�����??????����ˮ����ʵ���в���������������ŵ���ζ��������_________________�����Լ������Գ�ȥ��
��3��ij��ȤС���ͬѧ��ʵ��������ȡ����ϩ�г������������� �����������������ʵ��ͼ��ȷ�����������������C2H4��SO2���ش��������⣺
�����������������ʵ��ͼ��ȷ�����������������C2H4��SO2���ش��������⣺
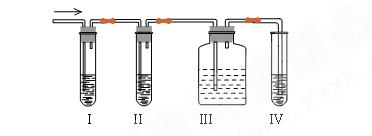
1��I��II��III��IVװ�ÿ�ʢ�ŵ��Լ�����Ϊ??? ????������ĸ��
????������ĸ��
��Ʒ����Һ??��NaOH��Һ?��Ũ����???������KMnO4��Һ
A���ܢڢ٢�
B���٢ڢ٢�
C���٢ڢ٢�
D���ܢڢ٢�
2����˵��SO2������ڵ�������????��
3��ʹ��װ��III��Ŀ����???????????��
4��ȷ��������ϩ��������??????????��
�ο��𰸣�( 14��)
��1���������������Һ��ˮ�� NaOH
�����������
�����Ѷȣ�һ��
3������� �������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
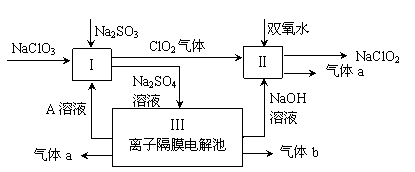
��1��˫��ˮ�ĽṹʽΪ��???????????�����з�����Ӧ�Ļ�ԭ�����������������ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ������������??????????????????????������ ��
��3��A�Ļ�ѧʽ���������������� ��װ�â���A���������������� ����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���
��д���÷�Ӧ�Ļ�ѧ����ʽ����������������
���о�����������Ӧ��ʼʱ����Ũ�Ƚϴ��������������Cl2�������ӷ���ʽ���Ͳ���Cl2��ԭ��������������????????????????????????����
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ���������????(����ͬ������ͬ�����ж�)
�ο��𰸣���14�֣���1��H-O-0-H?? Na2SO3������2�֣�
���������
�����������H2O2��������ԭ�Ӽ��γ�һ�����õ��Ӷԣ��ṹʽΪ��H�DO�DO�DH����ӦI��2ClO3�D��SO32�D��2H��=2ClO2��SO42�D��H2O������SO32�D��S��+4�۱��+6�ۣ�����ԭ�������Ϊ��H�DO�DO�DH��Na2SO3�����ƴ�ͼ�ж�����Ӧ��ΪClO2��H2O2,��������������ΪNaClO2��ClO2����������H2O2�����ɨD1�۱�ɨD2��2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���ʴ𰸣�2ClO2 + H2O2 + 2OH��= 2ClO2��+ O2��+ 2H2O���Ǣ�������2H2O�D4e�D=4H�� ��O2��,aΪO2,������4H2O��4e�D=4OH�D?��2H2��,?bΪH2�� A�Ļ�ѧʽ��H2SO4, װ�â���A���������������𰸣�H2SO4��������Cl�DŨ�ȴ�ʱ����ԭ����ǿ�������ɵ�ClO2������5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����Ϊ��5NaClO2 + 4HCl =" 5NaCl" + 4ClO2��+ 2H2O��ClO2��+ 3Cl��+ 4H+ = 2Cl2+ 2H2O����ClO2�D��ClO3�D��Fe2�� ��Ӧ���ն����Cl�D������ǰ��ת�Ƶĵ�������ͬ����������Fe2+�����ʵ�����ͬ���𰸣���ͬ��
�����Ѷȣ���
4��ʵ���� 15�֣�ij��ȤС��ͬѧ���������װ�ã����мг�������������������ȴˮ��û�л��������ü��ȱ����ᡢŨH2SO4���Ҵ������ķ������Ʊ������������������鷴Ӧ�IJ��ָ�����ұ����������ķе�Ϊ213�棬���ѵķе�Ϊ34.6�档

�Źرջ���a����ͨ��ֱ�����ܵ�����ˮ����A����30���ӣ��Ʊ�������E��������????????????��
��������Ӧ�ĸ���������У����ѣ�CH3CH2��O��CH2CH3������ϩ��SO2��ˮ�ȡ�
�ٴ���a������ֱ�������Ϸ��������ӣ�ͨ��B��C��Dװ�ü���SO2����ϩ����֪C��ʢ�ŵ��Լ���NaOH��Һ��B��D��Ӧʢ�ŵ��Լ����ηֱ���????????????????????????��
����ͬѧ��ͨ����������Ǽ������ò������Ƿ��С���CH2CH3������ȷ���������д������ѡ�����Ը�ͬѧ�Ĺ۵�������ۣ�???????????????????????????????��
��ͨ������ʵ�鷽���������ᴿ������������
��Ϊ��ȥ��Ʒ�����ʣ��Ƚ�������ƿ�в�Һ����ʢ����ˮ���ձ��У�������?????????��
���÷�Һ���ɷ��������л����ˮ�㣬��Һ��ɺ�ȡ���л���IJ�����???????????????��
������ƿ�м�������������С����ˮ�Ȼ��Ƹ���������Ѳ�����������˵��Ѳ㣬Ȼ���Ѳ���뵽�����������ƿ��������������п��Ƶ��¶�Ϊ????????��
�ο��𰸣���������������������������?�Ƣ�Ʒ�졢��ˮ��������KMnO
�����������1�����ڷ�Ӧ�е��л��Լ��ڼ��ȹ������ӷ���Ϊ��߲��ʣ������ܳ�������������Ҫ������������
��2������ϩ����һ��ͨ����ˮ��ɫ�����Ը��������Һ��ɫ��SO2�ļ���һ����Ʒ���Լ�����SO2Ҳ��ʹ��ˮ��ɫ�����Ը��������Һ��ɫ������Ҫ�ȼ���SO2�����ü�Һ���գ��ټ�����ϩ
��3���ᴿ���������������ü�Һ��Na2CO3��Һ��ȥ����ˮ�������ʣ����ý��з�Һ������ٶ��л������������뼴�ɡ�
�����Ѷȣ�һ��
5��ѡ���� ������ȡ�����ռ������е���������(a��b��c��ʾ��Ӧ�����м�����Լ�)���п��е���
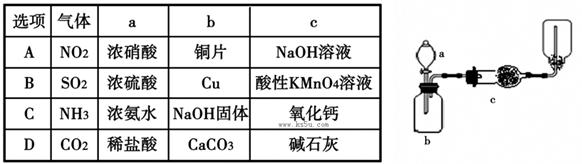
�ο��𰸣�C
���������
�����������ʵ��װ��ͼ��֪����װ��ΪҺ������壨��Һ�壩�ڲ����������·�Ӧ�Ʊ������װ�ã����������ܶȱȿ���С���������ſշ��ռ����ٽ�һ����������Ҫ�Ʊ�����ľ����Ƿ����������һ����װ��ͼ֪�������������ſշ��ռ���˵�����ܶȱȿ���С�����ѡ��ֻ�а������ܶȱȿ���С��ѡC�������������������A��NO2��NaOH��Ӧ�������գ�������NaOH��Һ����������װ��Ϊ�����ֻ��ʢ�Ź����Լ���NO2�ܶȱȿ��������������ſ������ռ�������B��Ũ���������ͭ�ķ�Ӧ���ڼ��ȵ������½��У�����ʵ��û�м��ȣ�SO2������KMnO4��Һ��Ӧ�������գ�����������KMnO4��Һ����������װ��Ϊ�����ֻ��ʢ�Ź����Լ���SO2�ܶȱȿ��������������ſ������ռ�������C�������ܶȱȿ���С�����������ſշ��ռ����������ù������������ȷ��D��������̼�����ʯ�ҷ�Ӧ�������ü�ʯ�Ҿ��������Ҷ�����̼�ܶȴ��ڿ����������������ſշ��ռ�������
�����Ѷȣ�һ��