微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验能证明有SO2存在的是(??? )
①能使澄清石灰水变浑浊?②能使湿润的蓝色石蕊试纸变红?③能使品红溶液褪色?④通入足量的NaOH溶液中再滴加BaCl2溶液有白色沉淀生成,该沉淀溶于稀盐酸?⑤通入溴水中能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀生成
A.都能证明
B.只有⑤能证明
C.③④⑤能证明
D.都不能证明
2、计算题 硫酸是化学工业中的重要原料,至2010年我国已成为全球硫酸产能最高、产量最大的国家。
(1)18.4mol/L(质量分数0.98,密度1.84g/cm3)浓硫酸是常用的干燥剂,用于吸收潮湿气体中的水蒸气。当浓硫酸浓度降到16 mol/L(密度1.8g/cm3)以下时,则失去干燥能力。
①16 mol/L的硫酸的质量分数为????????????(保留两位小数,下同)。
②50mL质量分数为0.98的浓硫酸作为干燥剂时,最多可吸水??????????????g。
(2)将铁粉与硫粉在隔绝空气条件下反应所得的固体M 9.920 g,与足量稀硫酸反应,收集到气体2.688 L(换算到标准状况),质量为3.440 g。则固体M的成分为
?????????(写化学式),其中铁元素与硫元素的质量比为????????????????。
(3)当代硫酸工业大多用接触法制硫酸(设空气中氧气的体积分数为0.20)。
①为使黄铁矿煅烧充分,常通入过量40%的空气,则煅烧后炉气中SO2的体积分数为????????????????????。
②将①中的炉气经净化除尘后直接送入接触室,流量为1.00m3/s,从接触室导出气体的流量为0.95m3/s(同温同压下测定),则SO2的转化率为????????????????%。
(4)接触法制硫酸排放的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2(循环利用)和混合铵盐。为测定此铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果如下:
铵盐质量为10.000 g和20.000 g时,浓硫酸增加的质量相同;
铵盐质量为30.000 g时,浓硫酸质量增重0.680 g;
铵盐质量为40.000 g时,浓硫酸的质量不变。
①计算该混合盐中氮元素的质量分数。
②计算上述氢氧化钠溶液的物质的量浓度。
3、选择题 铝制器皿能够盛放的物质是
A.KOH溶液
B.浓硫酸
C.NaOH溶液
D.稀硫酸
4、实验题 (10分)SO2是一种大气污染物,某兴趣小组欲探究SO2的性质及绿色实验方法,设计如下方案:
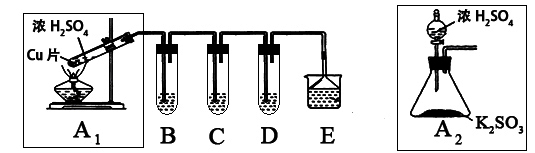
⑴ B、C、D分别用于检验SO2的漂白性、还原性和氧化性。其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为______________,C中反应的离子方程式为:____________________________________________。
⑵为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是:____________________________________________________(任写一点即可)。
⑶ E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO32-、SO42-、HSO3-等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为:小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2mol/L盐酸、2mol/L HNO3、1mol/L BaCl2溶液、1mol/L Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO32-和HSO3-,完成下表的实验操作、预期现象和结论:
实验操作
| 预期现象与结论
|
步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1mol/L BaCl2溶液向小烧杯滴加直至过量。
| 若出现白色浑浊,则溶液中存在SO32-或 SO42-。
|
步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体_______________
_______________________________________________________
| _________________________
____________________________
|
步骤3______________________________________________
____________________________________________________
| _________________________
_________________________
5、计算题 为15%、密度为1.31g/cm3的硫酸250mL(不含铁化合物或其它酸)跟过量的铁屑充分反应,计算:
(1)写出该反应的化学方程式????????????????????????????????????
(2)制得氢气(标准状况)的体积??????????????????????????
(3)把生成的硫酸亚铁配制成400mL溶液,这溶液的物质的量浓度是????????????。
|