��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������ɫ���̲�����Ϊ������ԭ��Ӧ����ɫ����
A����SO2����ͨ�뵽��ˮ��ʹ��ˮ��ɫ
B����SO2����ͨ�뵽KMnO4��Һ��ʹKMnO4����Һ��ɫ
C����SO2����ͨ�뵽���з�̪��NaOH��Һ�У���Һ��ɫ
D����SO2����ͨ�뵽��ˮ��ʹ��ˮ��ɫ
�ο��𰸣�C
���������SO2���л�ԭ�ԣ���ˮ���������Զ��߷�����������ԭ��Ӧ��ʹ��ˮ��ɫ�ģ�������ؾ���ǿ�����ԣ������������������ԭ��Ӧ�����������ɫ�������������������Ʒ�Ӧ�����������ƺ�ˮ��ʹ��Һ�ɼ��Ա�Ϊ���ԣ���̪�����˱�ɫ�����������˶�����������ԣ���ˮ����ǿ�����Զ���������л�ԭ�Զ��߷���������ԭ��Ӧʹ��ˮ��ɫ�����Դ�ѡC��
�����Ѷȣ���
2��ʵ���� ij�о�С����̽��SO2�Ļ�ѧ���ʣ����������ʵ�鷽����

(1)��B�м���SO2�������ԣ���B����ʢ�Լ���Ϊ________��
(2)��C��װFeCl3��Һ������SO2�Ļ�ԭ�ԣ���C�з�Ӧ�����ӷ���ʽΪ_____________________________________________________��
(3)��D��װ����Ư��Ũ��Һ��ͨ��SO2һ��ʱ���D�г����˴�����ɫ������ͬѧ�Ƕ�ɫ�����ɷֽ�����̽������ش��������⣺
��ѡ���������Լ�������װ�á��Թܡ��ιܡ������ܵĵ�����������ˮ��0.5 mol��L��1���ᡢ0.5 mol��L��1H2SO4��Һ��0.5 mol��L��1BaCl2��Һ��Ʒ����Һ�����Ƴ���ʯ��ˮ��
(��)����һ���ð�ɫ����ΪCaSO3��
��������ð�ɫ����Ϊ________��
���������ð�ɫ����Ϊ�����������ʵĻ���
(��)���ڼ���һ����д�±���
ʵ�����
| Ԥ������ͽ���
|
��D�г������ˣ�ϴ�Ӹɾ�����
| ?
|
����һ�ɾ��Թ�ȡ����������Ʒ������______________
| _________________________
?
(��)���������������д�����ɸð�ɫ�����Ļ�ѧ����ʽ��
__________________________________________________��
�ο��𰸣�(1)����ˮ��Һ(�����ơ����⻯�ƻ���Ӧ���ʵĻ�ѧʽ����
���������(1)��(2)�漰SO2������ʵ�顣SO2����������Ҳ�л�ԭ�ԣ�������ֻ�ԭ��(�ܹ�����������ǿ��Fe3����H2O2��ǿ������HClO������)��һ���ں�H2S�ȣ�2�����ﷴӦʱ�����������ԣ����B��ΪH2S(��Na2S��NaHS��)��Һ��
(3)̽����ɫ�����ijɷ֣���ʵ�Ǽ���SO32����SO42������ͨ������������ᷴӦ����SO2ʹƷ����Һ��ɫ������SO32����HSO3����
�����Ѷȣ�һ��
3��ѡ���� ����ͼ��ʾʵ��װ��(�г���������ȥ)̽��ͭ˿�����Ũ����ķ�Ӧ������ʵ�鲻��������
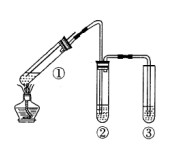
A�������ƶ�����ͭ˿�ɿ���SO2����
B������ѡ��Ʒ����Һ��֤SO2������
C������ѡ��NaOH��Һ���ն����SO2
D��Ϊȷ��CuSO4���ɣ�����м�ˮ���۲���ɫ
�ο��𰸣�D
���������
���������A�������ƶ�����ͭ˿����ͭ˿��Ũ����Ӵ��ͷ�����Ӧ�����뿪Һ�淴Ӧ��ֹͣ���ʿ��Կ���SO2��������ȷ��B��SO2��Ư���ԣ���ʹƷ����Һ��ɫ�����Ԣ���ѡ��Ʒ����Һ��֤SO2�����ɡ���ȷ��C��SO2�������������������Ӧ������ѡ��NaOH��Һ���ն����SO2����������ȫ����ȷ��D����Ӧ��װ���к���û��Ӧ���ȵ�Ũ���ᣬ����Ϊȷ��CuSO4���ɣ�Ӧ�ѷ�ӦҺ��ȴ����뵽ˮ�С���ע����ˮ������
�����Ѷȣ�һ��
4��ѡ���� ��֪A�ǵ��ʣ�E��ˮ��Һ��ǿ���ԡ�A��B��C��D��E�Ǻ���һ����ͬԪ�ص��������ʣ���һ�������¿ɷ������е�ת������A������
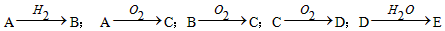 [???? ] [???? ]
A��Cl2
B��N2
C��S
D��C
�ο��𰸣�BC
���������
�����Ѷȣ���
5��ѡ���� ���з�Ӧ�У����������������(����)?
A��2HBr+H2SO4��Ũ��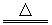 Br2+SO2��+2H2O? Br2+SO2��+2H2O?
B��Ca3��PO4��2+2H2SO4��Ũ�� 2CaSO4+Ca��H2PO4��2? 2CaSO4+Ca��H2PO4��2?
C��2Al+3H2SO4====Al2��SO4��3+3H2��?
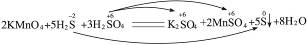
D��2KMnO4+5H2S+3H2SO4====K2SO4+2MnSO4+5S��+8H2O?
�ο��𰸣�BD
���������ֻҪH2SO4��ij��Ԫ�صļ�̬���ͣ���ʵֻ����H��SԪ�صļ�̬���ͣ���H2SO4������������A��SԪ����+6�۱䵽��+4�ۣ�C����HԪ����+1�۱䵽��0�ۣ�����������Ӧ�У�H2SO4������������A��C���ѡ��B�Ӧ����������ԭ��Ӧ��B���ѡ��D�Ӧ��HԪ�صļ�̬û�иı䣬SԪ�صı仯Ϊ��
H
�����Ѷȣ���
|