微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将1mol NaOH溶解后配制成1L溶液,该溶液中NaOH的物质的量浓度是

A.0.01mol/L
B.0.1mol/L
C.1mol/L
D.10mol/L
参考答案:C
本题解析:c===1mol/L
本题难度:简单
2、选择题 下列有关0.1mol?L-1 NaOH溶液的叙述正确的是( )
A.1L该溶液中含有NaOH 40g
B.100mL该溶液中含有OH-0.01mol
C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01mol?L-1
D.在1L水中溶解4gNaOH即可配制得0.1mol?L-1NaOH溶液
参考答案:A、1L0.1mol?L-1 NaOH溶液中含氢氧化钠的质量
本题解析:
本题难度:简单
3、选择题 下列有关阿伏伽德罗常数说法正确的是
A.含0.2mol H2SO4的浓硫酸与足量锌反应,生成气体的分子数小于0.1NA
B.标况下,22.4L四氯化碳所含分子数大于NA
C.0.1mol/L 的AgNO3溶液中,阳离子所带正电荷数目为0.1NA
D.电解267g熔融AlCl3,能生成3mol Cl2和54g金属铝
参考答案:B
本题解析:
试题分析:A、生成的气体的分子数为0.1NA,错误;B、四氯化碳标况下为液体,正确;C、未指明溶液的体积,故无法计算,错误。 D、AlCl3是共价化合物,错误。
本题难度:一般
4、选择题 以下有关物质的质量分数和物质的量浓度的叙述正确的是
A.等体积硫酸铁、硫酸铜、硫酸钾溶液分别与足量的氯化钡溶液反应,若生成硫酸钡沉淀的质量相等,则三种硫酸盐溶液的物质的量浓度之比为1:1:1
B.Na2O2和Na2O各0.1mol分别放入100g水中,所得溶液的物质的量浓度不相等
C.质量分数分别为5%和15%的氨水等体积混合后所得溶液的质量分数为10%
D.20℃时,饱和KCl溶液的密度为1.174g?cm-3,物质的量浓度为4.0 mol?L-1,则此溶液中KCl的质量分数为 ×100%
×100%
参考答案:D
本题解析:
试题分析:A项,由生成硫酸钡沉淀的质量相等,即生成硫酸钡的物质的量相等,说明各溶液中含有相量物质的量的SO42-,设溶液中含有的物质的为1 mol,则有Fe2(SO4)3  mol、CuSO41 mol、K2SO41 mol,故浓度之比为
mol、CuSO41 mol、K2SO41 mol,故浓度之比为 本题难度:一般
本题难度:一般
5、选择题 硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当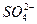 的浓度为0.20 mol・L-1时,加入等体积的0.20 mol・L-1的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是(???)
的浓度为0.20 mol・L-1时,加入等体积的0.20 mol・L-1的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是(???)
A.0.20 mol・L-1
B.0.25 mol・L-1
C.0.225 mol・L-1
D.0.45 mol・L-1
参考答案:C
本题解析:设原溶液为1 L,其中有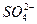 ?0.20 mol;由Al3+与OH-的反应关系可得原溶液中所含有的Al3+为0.05 mol,最后的溶液中,所含的溶质为K2SO4和KAlO2,它们的物质的量分别是0.20 mol和0.05 mol,则K+的总量为0.20 mol×2+0.05 mol="0.45" mol,c(K+)
?0.20 mol;由Al3+与OH-的反应关系可得原溶液中所含有的Al3+为0.05 mol,最后的溶液中,所含的溶质为K2SO4和KAlO2,它们的物质的量分别是0.20 mol和0.05 mol,则K+的总量为0.20 mol×2+0.05 mol="0.45" mol,c(K+)
本题难度:简单