微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1分)已知NaOH与NaHCO3发生反应的方程式为:

Ⅰ.实验室用氢氧化钠固体配制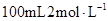 的NaOH溶液,回答下列问题:
的NaOH溶液,回答下列问题:
(1)下列操作的顺序是(每项限选一次)_____________。
A.称量
B.溶解
C.洗涤
D.定容
E.转移
F.摇匀
G.冷却
(2)若容量瓶中有少量蒸馏水,所配溶液的浓度将_____________;(填“偏大”、“偏小”或“无影响”)
(3)在定容操作时,俯视容量瓶刻度线,则所配溶液的浓度将_____________(填“偏大”、“偏小”或“无影响”)。
Ⅱ.在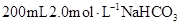 溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
溶液中加入一定量的常见纯净物X,恰好使其转化为只含Na2CO3溶质的溶液,实现转变的物质X有多种,请回答下列问题:
(1)请填写下表空白。
编号
| ①
| ②
| ③
| ④
|
X的化学式
|
| NaOH
| Na2O2
|
|
加入X的质量(g)
| 9.2
|
| 15.6
|
(2)反应后,溶液中的Na+的物质的量均为_____________mol。
(3)在①~④中,所得Na2CO3溶质的质量分数相等的是_____________(填编号)。
参考答案:Ⅰ.(1)A、B、G、E、C、D、F(1分)
(2)无
本题解析:
试题分析:Ⅰ.(1)配制溶液的顺序为称量,溶解,冷却,转移,洗涤,定容,摇匀,所以顺序为:A、B、G、E、C、D、F。(2)容量瓶中有水,对实验没有影响;(3)俯视时溶液的体积偏小,所得溶液的浓度偏大。Ⅱ.(1)碳酸氢钠的物质的量为2.0×0.2=0.4摩尔,加入物质X恰好转化为只含有碳酸钠溶质的溶液,则加的物质中只能是钠或氢氧化钠或氧化钠或过氧化钠,实际反应的实质为碳酸氢钠和氢氧化钠反应,需要0.4摩尔氢氧化钠。所以生成0.4摩尔氢氧化钠需要钠0.4摩尔,即0.4×23=9.2克,需要氢氧化钠0.4×40=1.6克,需要过氧化钠0.2摩尔,即0.2×78=15.6克,需要0.2摩尔氧化钠,即0.2×62=12.4克。所以填表为:
编号
①
②
③
④
X的化学式
Na
Na2O
加入X的质量(g)
1.6
12.4
(2)0.4摩尔碳酸氢钠反应后生成0.4摩尔碳酸钠,所以溶液中钠离子物质的量为0.8摩尔。(3)0.4摩尔钠会使溶液质量增加为9.2-0.4=8.8克,加入氢氧化钠的质量增加为16.0克,加入过氧化钠质量增加为15.6-3.2=12.4克,加入氧化钠的质量增加为12.4克,所以加入过氧化钠和加入氧化钠后溶液质量相等,所以碳酸钠的质量分数相等,选③和④。
考点:溶液的配制,钠的化合物的性质和相互转化。
本题难度:困难
2、选择题 某学生配制氯化钠溶液时,用天平称取氯化钠固体20.6 g,(1g以下由游码提供),因砝码与氯化钠的位置放反了,天平恰好平衡,用称量的该氯化钠配制溶液,则所配溶液浓度[???? ]
A.偏高
B.偏低
C.无影响
D.无法确定
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列说法中正确的是 ( )
A.1mol任何气体的体积都约为22.4L
B.1mol气态物质,当体积约为22.4L时,该气体一定处于标准状况下
C.在标准状况下,2mol酒精的体积约为44.8L
D.常温常压下,48gO3和O2的混合气体中含有的氧原子数为3NA
参考答案:D
本题解析:略
本题难度:一般
4、选择题 下列溶液中的氯离子数目与50 mL 1 mol・L-1的AlCl3溶液中氯离子数目相等的是( )
A.150 mL 1 mol・L-1的NaCl
B.75 mL 1 mol・L-1的FeCl3
C.150 mL 3 mol・L-1的KCl
D.75 mL 2 mol・L-1的CaCl2
参考答案:A
本题解析:
试题分析:50 mL 1 mol・L-1的AlCl3溶液中氯离子数目为1 mol・L-1×0.05L×3 = 0.15mol。A选项中氯离子数目为0.15mol。B选项中氯离子数目为0.225mol。C选项中氯离子数目为0.45mol。D选项中氯离子数目为0.3mol。
考点:物质的量浓度计算。
本题难度:一般
5、选择题 设NA表示阿伏加德罗常数的数值,下列叙述中正确的是 (???? )
A.1 mol NH3所含有的原子数为NA
B.常温常压下,22 .4 L氧气所含的原子数为2NA
C.在标准状况下,18g H2O所含的氧原子数为NA
D.物质的量浓度为0.5mol/L的MgCl2溶液中,所含Cl-的个数为NA
参考答案:C
本题解析:略
本题难度:一般
|