��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X��g��+3Y��g�� 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��
2Z��g�����˷�Ӧ�ﵽƽ��ı�־��
A���������ܶȲ���ʱ��仯
B�������ڸ����ʵ�Ũ�Ȳ���ʱ��仯
C��������X��Y��Z��Ũ��֮��Ϊ1��2��2
D����λʱ������0.1 mol Xͬʱ����0.2 mol Z
�ο��𰸣�B
���������
����������ж�һ����Ӧ�Ƿ�ﵽƽ��״̬��ʵ�������淴Ӧ������ȣ���־�����������Ƿ�ӡ��䡱�ﵽ�����䡱��A���ܶȦ�=m/V,m���䣬����ΪaL�ܱ����������ܶ���ʼ����û�б仯��C�и����ʵ�Ũ��֮�����жϷ�Ӧ�Ƿ�ﵽƽ��״̬��D���DZ�ʾ����Ӧ����Ӧ�ﵽƽ��״̬��Ҫ���淴Ӧ������ȣ���D����
�������ж�һ����Ӧ�Ƿ�ﵽƽ��״̬��������߿����ص㡣�����ڱ���������Ӧץסʵ�ʡ�ͨ����־���з������Ѷ��еȣ�һ����ѡ������֡�
�����Ѷȣ���
2��ѡ���� ��һ���¶��£���a L�ܱ������м���1 mol X�����2 mol Y���壬�������·�Ӧ��X��g����2Y��g��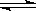 2Z��g�����˷�Ӧ�ﵽƽ��ı�־��??
2Z��g�����˷�Ӧ�ﵽƽ��ı�־��??
A��������ѹǿ����ʱ��仯