��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij��ѧ����С���о���������������ʱ���ı�ijһ�����Ի�ѧƽ���Ӱ�죬�õ����±仯���ɣ�ͼ��P��ʾѹǿ��T��ʾ�¶ȣ�n��ʾ���ʵ�����
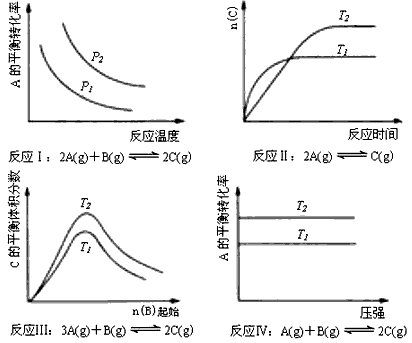
�������Ϲ����жϣ����н�����ȷ����[???? ]
A����Ӧ��H>0, P2>P1
B����Ӧ��H<0, T1<T2
C����Ӧ��H>0, T2>T1; ���H<0, T2<T1
D����Ӧ������H<0, T2> T1
�ο��𰸣�BC
���������
�����Ѷȣ�һ��
2��ѡ���� T��ʱ����1L���ܱ������г���2mol?CO2��6mol?H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������H=-49.0kJ?mol-1���H2��CH3OH��g����Ũ����ʱ��仯����ͼ��ʾ������˵������ȷ���ǣ�������
| ʱ�� | c?��H2��/mol?L-1 | c?��CH3OH��/mol?L-1 | v��������v?���棩
�Ƚ�
?t0
6
0
��
t1
3
1
v������=v���棩
A��t0��t1ʱ���ڦԣ�H2��=3
t1-t0
?mol?��L?min��-1
B��t1ʱ���������¶Ȼ��ٳ���CO2���壬���������H2��ת����
C��t0ʱ��v��������v���棩
D��T��ʱ��ƽ�ⳣ��K=1/27��CO2��H2��ת�������
�ο��𰸣�A��t0��t1ʱ���ڦԣ�H2��=
���������
�����Ѷȣ���
3��ѡ���� ��mA��������nB������ pC��������qD��������Ӧ�У���10min��ƽ�⣬��ʱ�����ʵ�Ũ�ȱ仯Ϊ��A����amol/L��B����a/3?mol/L��C����2a/3?mol/L����ʱ������ϵ��ѹ����ѧƽ�ⲻ�ƶ�����m��n��p��qΪ???????????????????????????[???? ] pC��������qD��������Ӧ�У���10min��ƽ�⣬��ʱ�����ʵ�Ũ�ȱ仯Ϊ��A����amol/L��B����a/3?mol/L��C����2a/3?mol/L����ʱ������ϵ��ѹ����ѧƽ�ⲻ�ƶ�����m��n��p��qΪ???????????????????????????[???? ]
A.1��1��1��1????????????????????????
B.1��3��3��1
C.1��3��2��2????????????????????????
D.3��1��2��2
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4��ѡ���� һ�������£����淴ӦN2+3H2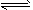 2NH3������ӦΪ���ȷ�Ӧ���ﵽƽ�⣬�������ı������������й������������[???? ] 2NH3������ӦΪ���ȷ�Ӧ���ﵽƽ�⣬�������ı������������й������������[???? ]
A���Ӵ�����V����V�涼�����仯���ұ仯�ı������
B����ѹ��V����V�涼������V������ı�������V������ı���
C�����£�V����V�涼��С����V����С�ı�������V���С�ı���
D����������Ũ�ȣ�V����V�涼������V������������V����������N2ת���ʼ�С��H2ת��������
�ο��𰸣�C
���������
�����Ѷȣ�һ��
5������� �ҹ��Ǹ������������������Ϊ�����һ����¯��������Ϊ�ձ������������
I����֪��
2CO(g)��O2(g)��2CO2(g)??��H����566kJ/mol?
2Fe(s)+3/2O2(g)��Fe2O3(s)?��H����825.5?kJ/mol
��Ӧ��Fe2O3(s)��3CO(g)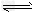 2Fe(s)��3CO2(g)??��H��_______kJ/mol�� 2Fe(s)��3CO2(g)??��H��_______kJ/mol��
II����Ӧ?1/3Fe2O3(s)��CO(g)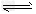 2/3?Fe(s)��CO2(g)��1000���ƽ�ⳣ������4.0����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����10min��ﵽƽ�⡣ 2/3?Fe(s)��CO2(g)��1000���ƽ�ⳣ������4.0����һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0mol����Ӧ����10min��ﵽƽ�⡣
(1)CO��ƽ��ת����=?_____________��
(2)�����CO��ƽ��ת���ʣ��ٽ�Fe2O3��ת�����ɲ�ȡ�Ĵ�ʩ��________
a����߷�Ӧ�¶�????b������Ӧ��ϵ��ѹǿ c��ѡȡ���ʵĴ���???
d����ʱ���ջ��Ƴ�����CO2? e�������ʯ��ʹ����ƽ���������ֽӴ�
III��(1)��¯���������ķ����е�CO�ɽ��л��գ�ʹ����һ�������º�H2��Ӧ�Ʊ��״���
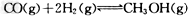 ??�������ͼʾ�ش��������⣺ ??�������ͼʾ�ش��������⣺
(1)�ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����?(H2)=?________��
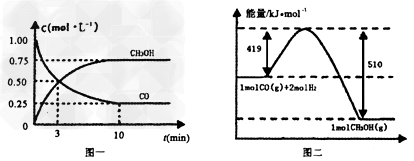
(2)�����¶Ⱥ�������ͬ�������ܱ�������,����ͬ��ʽͶ�뷴Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±�
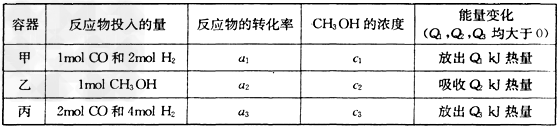
�����й�ϵ��ȷ����________��
A��c1=c2 B��2Q1=Q3 C��2a1=a3 D��a1?+a2?=1
E���÷�Ӧ������1mol?CH3OH����ų�(Q1+Q2)kJ����
(3)����һ����ɱ���ܱ������г���l?molCO��2mol?H2��1mol?CH3OH���ﵽƽ�ⅼ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ��________(����������桱)��Ӧ�����ƶ���
(4)�״�������������ȼ�ϵ�أ��õ���ö�Ķ��Ե缫����Ũ����������Һ��д���õ�صĸ�����Ӧʽ__________________��
�ο��𰸣�I��-23.5?
II��(1)?60����(2)d
���������
�����Ѷȣ�һ��
|
|