微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,22.4LH2含有的分子数为NA
B.25℃、101KPa时,1 mol CO2气体所占有的体积约为22.4L
C.标准状况下,4.0g NaOH含有的Na+ 离子数为0.1 NA
D.物质的量浓度为0.5mol /L的MgCl2溶液中,含有Cl―个数为1 NA
参考答案:C
本题解析:
试题分析:A.不是标准状况下,无法确定气体的物质的量,错误;B.标准状况是0℃、101Kpa,25℃、101KPa时,不是标准状况下,无法确定气体的体积,错误;C.4g氢氧化钠的物质的量为0.1mol,0.1mol氢氧化钠中含有0.1mol钠离子,含有的Na+离子数为0.1NA,正确;D.体积未知,无法计算含有Cl―的数目,错误。
考点:阿伏加德罗常数、气体摩尔体积等。
本题难度:一般
2、选择题 等质量的①CH4、②H2、③HCl、④SO2,在标况下所占体积由大到小排列的顺序是
A ②>①>③>④????????????????????????? B ④>③>①>②.
C ③>②>④>①????????????????????????? D ①>④>②>③
参考答案:A
本题解析:标准状况下气体体积越大则气体物质的量最大,在等质量的情况下,摩尔质量越小,即相对分子质量最小物质的量的最大,所以正确的排序为:②>①>③>④
本题难度:简单
3、填空题 欲用98%的浓硫酸(p=1.84g・cm-3 )配制成浓度为0.5mol・L-1的稀硫酸500ml。
(1)选用的主要仪器有:
①__________,②__________,③__________,④____________,⑤____________。
(2)请将下列各操作,按正确的序号填在横线上。
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加蒸馏水至刻度线
D.洗净所用仪器
E.稀释浓H2SO4
F.将溶液转入容量瓶
其操作正确的顺序依次为__________ __________________。
(3)简要回答下列问题:
①所需浓硫酸的体积为____________mL。
②如果实验室有15mL、20mL、50mL的量筒应选用____________mL的量筒最好.
(4)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了_________________________。
(5)在配制过程中,①某学生观察定容时仰视液面,所配溶液的浓度会________(填“偏高”、“偏低”或“无影响”下同)。②未经冷却趁热将溶液注入容量瓶中,________。③摇匀后发现液面低于刻度线再加水,________。④容量瓶中原有少量蒸馏水,________。
参考答案:(1)量筒 烧杯
本题解析:
试题解析:(1)操作步骤有计算、量取、稀释、洗涤、定容、摇匀等操作,一般用量筒量取浓硫酸,在烧杯中稀释(可用量筒量取水加入烧杯),并用玻璃棒搅拌.冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有量筒、烧杯、玻璃棒、500mL容量瓶、胶头滴管.故答案为:量筒;烧杯;玻璃棒;500mL容量瓶;胶头滴管;(2)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:AEFDCB;
(3)浓硫酸的物质的量浓度为c=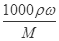 =
=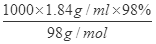 =18.4mol/L,设需要的浓硫酸额体积为Vml,根据溶液稀释定律C浓V浓=C稀V稀可知:18.4mol/L×Vml=0.5mol?L-1×500mL,解得V=13.6mL,根据“大而近”的原则,根据需要量取的浓硫酸的体积为13.6mL可知选用15mL量筒,故答案为:13.6;15;(4)在转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了保证溶质完全转移;(5)①某学生观察定容时仰视液面,则加水的量偏多了,所配溶液的浓度会偏低,②未经冷却就直接定容配置将使浓度,待冷却后溶液体积偏小,则浓度偏高;③摇匀后发现液面低于刻度线再加水,则加水的量偏多了,所配溶液的浓度会偏低;④容量瓶中原有少量蒸馏水,所配溶液的浓度无影响。
=18.4mol/L,设需要的浓硫酸额体积为Vml,根据溶液稀释定律C浓V浓=C稀V稀可知:18.4mol/L×Vml=0.5mol?L-1×500mL,解得V=13.6mL,根据“大而近”的原则,根据需要量取的浓硫酸的体积为13.6mL可知选用15mL量筒,故答案为:13.6;15;(4)在转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了保证溶质完全转移;(5)①某学生观察定容时仰视液面,则加水的量偏多了,所配溶液的浓度会偏低,②未经冷却就直接定容配置将使浓度,待冷却后溶液体积偏小,则浓度偏高;③摇匀后发现液面低于刻度线再加水,则加水的量偏多了,所配溶液的浓度会偏低;④容量瓶中原有少量蒸馏水,所配溶液的浓度无影响。
考点:一定物质的量浓度溶液的配制
本题难度:一般
4、选择题 若阿伏加德罗常数的数值用NA表示,下列说法正确的是( )
A.标准状况下,1.12L氦气所含原子数为0.1NA
B.1.6gNH2-离子所含质子数为NA
C.22.4 LHCl溶于水,溶液中H+数为NA
D.9g D2O所含的中子数为4.5NA
参考答案:D
本题解析:
试题分析:A、标准状况下1.12L的氦气的物质的量是0.05mol,氦气是单原子分子,所以所含原子数为0.05NA,错误;B、1.6g的NH2-离子的物质的量是0.1mol,1个NH2-离子中含有9个质子,所以所含质子数是0.9NA,错误;C、未指明标准状况,所以22.4L的HCl的物质的量不是1mol,溶液中的H+数不是NA,错误;D、9g D2O的物质的量是9/20mol,1个 D2O中的中子数是10,所以所含中子的物质的量是9/20mol×10=4.5mol,即中子数4.5NA,正确,答案选D。
考点:考查阿伏伽德罗常数的应用
本题难度:一般
5、选择题 VmL硫酸铁溶液中含wg SO42
参考答案:
本题解析:
本题难度:一般