微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (14分)化学反应速率和限度是中学化学原理中很重要部分,根据所学知识回答下列问题:
I、用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
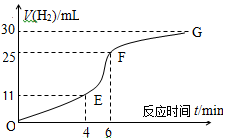
(1)实验过程如图所示,分析判断?????????段化学反应速率最快。
(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是?????????????????????????,一定时间后反应速率逐渐减慢,其原因是????????????。
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是(???????? )
A.蒸馏水
B.氯化钠固体
C.氯化钠溶液
D.浓盐酸 E.降低温度
II、某温度时,在2L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
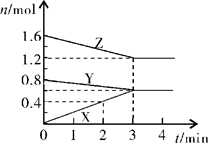
(1)该反应的化学方程式:????????????????????????????????;
(2)反应开始至2min末,X的反应速率为???????(mol・L-1・min-1);
(3)3min后图中曲线所表示的含义是??????????????????????。
参考答案:(14分) ?I、(1)EF;(2)该反应放热,体系温度升高
本题解析:I、(1)根据图像可知,EF段斜率最大,所以反应速率最快。
(2)由于该反应放热,体系温度升高,反应速率加快。但当反应进行到一定程度后,盐酸到浓度降低,此时浓度对反应速率的影响超过了温度对反应速率的影响,所以反应速率又逐渐降低。
(3)AC均是稀释,氢离子的浓度降低,反应速率降低。同样降低温度,反应速率也会降低。B对反应速率不影响,D是最大氢离子浓度,反应速率增大。答案选ACE。
II、 (1)根据图像可知,当反应达到平衡时,X的我这里增加了0.6mol,Y的物质的量减少了0.2mol,
本题难度:一般
2、选择题 下列有关化学反应速率的说法正确的是( )
A.凡是能量达到活化能的分子发生的碰撞均为有效碰撞
B.增大反应物浓度能加快正反应的反应速率,降低逆反应的反应速率
C.温度升高使化学反应速率加快的主要原因是增加了反应物分子之间的碰撞次数
D.决定化学反应速率的根本因素是参加反应的各物质的性质
参考答案:A.能量达到活化能的分子为活化分子,当活化分子发生碰撞能发生
本题解析:
本题难度:一般
3、选择题 下列因素能改变化学反应的活化能的是( )
A.温度
B.压强
C.反应物的浓度
D.催化剂
参考答案:温度、浓度、压强只改变活化分子的百分数或浓度,不能改变活化能
本题解析:
本题难度:一般
4、选择题 NO和CO都是汽车尾气里的有害物质,它们能缓慢反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是( )
A.使用催化剂不改变反应速率
B.改变温度对反应速率无影响
C.升高温度能加快反应速率
D.使用催化剂能加快反应速率
参考答案:加入催化剂,可降低反应的活化能,增大活化分子的百分数,增大反
本题解析:
本题难度:一般
5、选择题 为了减缓石灰石与盐酸的反应速率,可采取的方法是
A.将石灰石磨成粉未
B.向盐酸溶液中加入氯化钠溶液
C.加入浓盐酸
D.加热
参考答案:B
本题解析:
试题分析:在其它条件不变的情况下,减小浓度或降低温度或减小固体反应物的接触面积,均可以降低反应速率。所以为了减缓石灰石与盐酸的反应速率,可采取的方法是向盐酸溶液中加入氯化钠溶液,即相当于是稀释,盐酸的浓度降低,反应速率降低。其余选项均是加快反应速率,答案选B。
点评:该题是高考中的常见题型,属于中等难度的试题。试题贴近高考,基础性强。该题的关键是明确影响反应速率的外界条件,以及外界条件是如何影响反应速率的,然后结合题意灵活运用即可。
本题难度:一般