微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
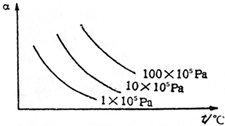
1、选择题 如图纵坐标为反应物的转化率α,横坐标为温度(t℃),下列符合此图情况的反应是( )
A.C(s)+CO2(g)
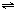
2CO(g);正反应吸热
B.H2(g)+Br2(g)
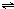
2HBr(g);正反应放热
C.N2(g)+3H2(g)
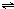
2NH3(g);正反应放热
D.2SO3(g)
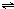
2SO2(g)+O2(g);正反应吸热
参考答案:C
本题解析:
本题难度:简单
2、选择题 化学平衡常数(K)、弱酸的电离常数(Ka)、难溶物的溶度积常数(Ksp)是判断物质性质或变化的重要的平衡常数。下列关于这些常数的说法中,正确的是 [???? ]
A.平衡常数的大小与温度、浓度、压强、催化剂等有关
B.当温度升高时,弱酸的电离常数Ka变小
C.Ksp(AgCl)>Ksp(AgI),由此可以判断AgCl(s)+I-=AgI(s)+Cl-能够发生
D.Ka(HCN)<Ka(CH3COOH),说明相同物质的量浓度时,氢氰酸的酸性比醋酸强
参考答案:C
本题解析:
本题难度:一般
3、选择题 T℃时,在2L密闭容器中X(g)与Y(g)反应生成Z(g),浓度变化如图1所示;若其他条件不变,温度为T1和T2时Y的体积百分含量与时间关系如图2所示.下列结论正确的是( )
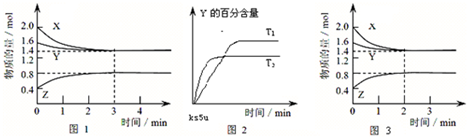
A.容器中的反应可表示为:3X(g)+Y(g)?2Z(g)
B.图1中,前3?min内X的反应速率为?v(X)=0.3mol/(L?min)
C.若其他条件不变,升高温度时反应的平衡常数K值变大
D.若改变条件,反应进程如图3所示,则改变的条件是增大体系的压强
参考答案:A、由图1知,X的物质的量减少量=(2.0-1.4)mol=
本题解析:
本题难度:简单
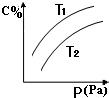
4、选择题 在密闭容器中,对于可逆反应A+3B?
 2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
2C(g),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是( )
A.A一定为气体
B.B一定为气体
C.该反应是放热反应
D.若正反应方向△H<0,则T1>T2
参考答案:B
本题解析:
本题难度:简单
5、选择题 一定温度下,反应N2(g)+3H2(g)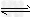 ?2NH3(g)的反应热和化学平衡常数分别为△H和K,?则相同温度时反应4NH3(g)
?2NH3(g)的反应热和化学平衡常数分别为△H和K,?则相同温度时反应4NH3(g) ?2N2(g)+6H2(g)反应热和化学平衡常数为 [???? ]
?2N2(g)+6H2(g)反应热和化学平衡常数为 [???? ]
A.2△H和2K????????????????????????
B.-2△H和?K2?
C.-2△H和?K-2???????????????????????
D.2△H和-2K?
参考答案:C
本题解析:
本题难度:一般