逐滴滴加氨水先有沉淀产生,后沉淀消失
参考答案: 本题解析:考查离子的共存。离子间如果能够发生化学反应,则不能大量共存,反之是可以的。选项A中如果钾离子浓度小于氯离子浓度,则不能符合电荷守恒定律,A不正确;B中Fe3+和I-以及HCO3-不能大量共存;C中氢氧化钠首先和醋酸反应,开始没有气体生成,所以正确的答案选D。 本题解析:考查离子的共存。离子间如果能够发生化学反应,则不能大量共存,反之是可以的。选项A中如果钾离子浓度小于氯离子浓度,则不能符合电荷守恒定律,A不正确;B中Fe3+和I-以及HCO3-不能大量共存;C中氢氧化钠首先和醋酸反应,开始没有气体生成,所以正确的答案选D。
小结:离子不能大量共存的一般情况是(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质)。(2)能生成微溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-)。(3)能完全水解的离子之间,如多元弱酸和弱碱盐
本题难度:一般
2、选择题 某种溶液仅含下表离子中的5种(不考虑水的电离与离子水解),且各种离子的物质的量均为1mol。
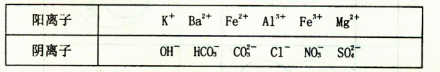
若向原溶液中加入足量的盐酸,有无色气体生成。经分析反应后溶液中阴离子的种类没有变化。则该溶液含有的离子组成为
A.Cl-、NO3-、SO42-、Fe2+、Mg2+
B.HCO3-、Cl-、CO32-、Fe2+、Mg2+
C.SO42-、CO32-、NO3-、Cu2+、Fe2+
D.Al3+、K+、Cl-、NO3-、SO42-
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列有关叙述正确的是
A.某无色溶液中加入足量稀HCl,有气体产生,且该气体能使澄清石灰水变浑浊,则该溶液中一定含有CO32-
B.某溶液中加入BaCl2溶液有白色沉淀产生,再加入稀硝酸白色沉淀不溶解,则原溶液中一定含有SO42-
C.某溶液中加入NaOH溶液产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定含有NH4+
D.某气体通入到品红溶液中,品红溶液褪色,则该气体一定是SO2
参考答案:C
本题解析:
试题分析:A不正确,也可能含有碳酸氢盐或亚硫酸盐;B不正确,因为氯化银也不溶于硝酸中;D不正确,因为氯气也能使品红溶液褪色,答案选C。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生能力的培养与解题方法的指导与训练,有利于培养学生严谨规范的实验设计能力。该类试题需要明确的进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:简单
4、填空题 现有A、B、C、D、E、F六种物质的溶液,分别为NH3・H2O、NaHSO4、AlCl3、AgNO3、NaAlO2、NaOH中的一种,已知:
①将A溶液逐滴滴加到B溶液中至过量,先出现沉淀,后沉淀溶解;
②将C溶液逐滴滴加到D溶液中至过量,先出现沉淀,后沉淀溶解;
③将E溶液逐滴滴加到F溶液中至过量,先出现沉淀,后沉淀溶解;
④在①和③的反应中出现的沉淀是同一种物质;
⑤A、D、F三种溶液呈酸性。
请回答下列问题:
(1)写出下列化学式:A ;D ;E 。
(2)过量A溶液与B溶液反应的离子方程式为 。
(3)将C溶液逐滴滴加到F溶液中至过量,此过程中反应的离子方程式为
。
(4)若A、C的混合溶液呈中性,则该溶液中所有离子的浓度的大小关系为
。
参考答案:(1)NaHSO4、AgNO3、NaOH(各2分)
本题解析:略
本题难度:一般
5、简答题 常温下,下列各组离子在给定条件下能大量共存的是( )
A.在pH=13的溶液中:NH4+、K+、ClO一、Cl-
B.在滴加石蕊试液显红色的溶液中:K+、NH4+、CO32-、SO42一
C.有NO3-存在的溶液中:H+、Ba2+、Cl一、SO32-
D.在c(H+)=1.0×10-3mol?L-1的溶液中:Na+、K+、SO42-、Al3+
参考答案:A.pH=13的溶液,显碱性,NH4+、OH-结合生成弱电解
本题解析:
本题难度:一般
|