微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列化学用语正确的是
A.乙醇的结构筒式:C2H6O
B.CH4的比例模型: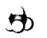
C.工业上制取粗硅的化学方程式:SiO2+C Si+CO2↑
Si+CO2↑
D.电解饱和食盐水的离子方程式:Cl-+2H2O=Cl2↑+2OH-+H2↑
参考答案:B
本题解析:
试题分析:A、乙醇的结构筒式为CH3CH2OH,C2H6O表示分子式,A不正确;B、CH4的比例模型为 ,B正确;C、工业上制取粗硅的化学方程式:SiO2+2C
,B正确;C、工业上制取粗硅的化学方程式:SiO2+2C
本题难度:一般
2、选择题 下列物质溶于水,不发生氧化还原反应的是
A.NO2溶于水
B.Na2O2溶于水
C.Cl2溶于水
D.CaO溶于水
参考答案:D
本题解析:
试题分析:A.NO2溶于水3NO2+ H2O = 2HNO3+ NO,有元素化合价的升降,是氧化还原反应。错误。B.Na2O2溶于水2Na2O2+2H2O="4NaOH+" O2↑。有元素化合价的升降,是氧化还原反应。错误。C.Cl2溶于水Cl2+H2O HCl+HClO,元素的化合价发生了变化,是氧化还
HCl+HClO,元素的化合价发生了变化,是氧化还
本题难度:一般
3、选择题 将足量的铜屑加入到100 mL浓度均为2 mol・L-1的HNO3和H2SO4的混合溶液中,充分反应后,转移电子的物质的量为 ( )
A.0.6 mol
B.0.8 mol
C.0.45 mol
D.0.4 mol
参考答案:C
本题解析:
试题分析:100 mL浓度均为2 mol・L-1的HNO3和H2SO4的混合溶液中n(H+)="0.1L×2" mol・L-1+0.1L×2 mol・L-1×2=0.6mol,n(NO3-)="0.1L×2" mol・L-1=0.2mol,根据反应3Cu+2NO3-+8H+=3Cu2++2NO↑+4 H2O可知氢离子不足,所以按氢离子的量进行计算,则生成NO的物质的量是0.6mol/4=0.15mol,所以转移电子的物质的量是0.15mol×3=0.45mol,答案选C。
考点:考查金属与混酸的计算
本题难度:一般
4、选择题 芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:SiO2 + 2C ="===" Si +2CO↑,该反应的基本类型是
A.化合反应
B.分解反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:
正确答案:C
SiO2 + 2C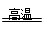 Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
Si +2CO是化合物+单质=化合物+单质的反应,是置换反应,C正确。
本题难度:简单
5、简答题 镁、铝合金3g与100mL稀H2SO4恰好完全反应,将反应后所得溶液蒸干,得无水硫酸盐17.4g,则原硫酸溶液的物质的量浓度为( )
A.1.5mol/L
B.1mol/L
C.2.5mol/L
D.2mol/L
参考答案:17.4g为硫酸镁和硫酸铝的质量,
由于镁、铝合金3g
本题解析:
本题难度:一般