微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
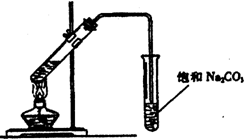
1、简答题 实验室用如图所示装置制取乙酸乙酯.
(1)装置中通有蒸气的导管要插在饱和Na2CO3溶液的液面上,不能插入溶液中,目的是:______;
(2)饱和Na2CO3溶液的作用是:______;
(3)实验生成的乙酸乙酯,其密度比水______.(填“大”或“小”);
(4)分离乙酸乙酯和饱和Na2CO3溶液所需要的主要仪器是:______.
2、简答题 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式______;
(2)浓硫酸的作用是:①______;②______;
(3)饱和碳酸钠溶液的主要作用是______;
(4)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止______.
(5)若要把制得的乙酸乙酯分离出来,应采用的实验操作是______.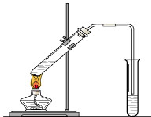
3、实验题 下图为苯和溴的取代反应的改进实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。
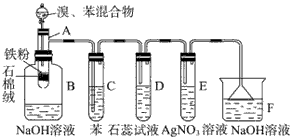
完成下列问题:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):______________________。
(2)试管C中苯的作用是______________________。反应开始后,观察D和E两试管,看到的现象为______________________。
(3)反应2 min-3 min后,在B中的NaOH溶液里可观察到的现象是____________________。
(4)在上述整套装置中,具有防倒吸作用的仪器有__________ (填字母)。
(5)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是____________________。
4、实验题 纳米碳酸钙广泛应用 于橡胶,塑料、造纸、化学建材、油墨、涂料、密封胶与胶粘剂等行业。在浓
CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。某校学生实验小组设计如图所示装置,制取该产品。D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去。
Ⅰ.可选用的药品有:a.石灰石 b.饱和氯化钙溶液 c.6 mol/L盐酸 d.氯化铵 e.氢氧化钙。

(1)A中制备气体时,所需药品是(选填字母序号)________;
(2)B中盛有饱和碳酸氢钠溶液,其作用是________________;
(3)写出制取氨气的化学方程式:____________________;
(4)在实验过程中,向C中通入气体式有先后顺序的,应先通入气体的化学式:___________________;
(5)检验D出口处是否有氨气逸出的方法是________________;
(6)写出制纳米级碳酸钙的化学方程式:____________________;
(7)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级_______________
(8)若实验过程中有氨气逸出,应选用下列____装置回收(填代号)。

Ⅱ.经分析在上述氯化铵样品中含有杂质碳酸氢钠。为了测定氯化铵的质量分数,该学生实验小组又设计了如下实验流程
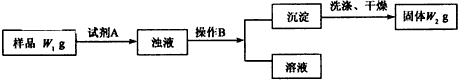
试回答:
(9)所加试剂A的化学式为________,检验所加试剂A已经过量的方法是____________。
(10)B操作方法是________,洗涤沉淀的方法是________。
(11)样品中氯化铵的质量分数为________。
5、填空题 氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K。工业上制备无水FeCl3的一种工艺如下:
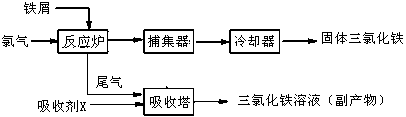
无水FeCl3的一种工艺如下:
(1)取0.5mL三氯化铁溶液滴入50mL沸水中,再煮沸片刻得红褐色透明液体,该过程可用离子方程式表示为:________________________ 。
(2)已知六水合氯化铁在水中的溶解度如下:
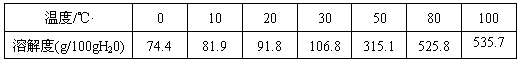
从FeCl3溶液中获得FeCl3・6H2O的方法是:_________________ 。
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:___________
(4)室温时在FeCl3溶液中滴加NaOH溶液,当溶液pH为2.7时,Fe3+开始沉淀;当溶液pH为4时,c(Fe3+)= ______________mol/L(已知:Ksp[Fe(OH)3]= 1.1×10-36)。
(5)吸收剂X是: ____________;吸收塔中吸收剂X的作用是:_____________________ 。
(6)FeCl3的质量分数通常可用碘量法测定:称取m克无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用cmol/LNa2S2O3溶液滴定,反应方程式为:I2+2S2O32-=2I-+S4O62-,共用去VmL。则样品中氯化铁的质量分数为:______________。