��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��98%��Ũ���ᣨ���ܶ�Ϊ1.84g/cm3������100mL1.0mol?L-1ϡ���ᣮ
��1������ȡŨ��������Ϊ______mL������һλС����
��2����ʵ�������У���A��100mL��Ͳ��B��������ƽ��C����������D��50mL����ƿ��E��10mL��Ͳ?��F����ͷ�ι�?��G��50mL�ձ�?��H��100mL����ƿ
ʵ��ʱѡ�õ�������C��F��G�Ӧѡ��______������ţ�
��3�����ƹ����У����������ʹ���ƽ��ƫ�ߵ���______������ţ�
��A������ʱ���ӿ̶��߹۲�Һ�棻??��B������ƿʹ��ʱδ���
��C�����ݺ���ҡ�ȡ����ã�����Һ����ڿ̶��ߣ��ټ�����ˮ�����̶���
��4��������ƿ��ʹ���У����в�������ȷ����______������ţ�
��A��ʹ������ƿǰ������Ƿ�©ˮ
��B������ƿ������ˮϴ�����ô����Ƶ���Һϴ��
��C�����������ƹ��������ƽ���̵���ֽ�ϣ�ȷ�����������ձ����ܽ������ע������ƿ��
��D����ȷ��ȡ��18.4mol?L-1�����ᣬע����ʢ��30mLˮ��100mL������ƿ�У���ˮ���̶���
��5��������ʱ����μ�����ˮ�����Գ���������ƿ�̶��ߣ���ʱʵ��Ӧ��μ������У�
��______��
�ο��𰸣���1��Ũ��������ʵ���Ũ��C=
���������
�����Ѷȣ�һ��
2������� �������֣���1��30%��H2SO4��50%��H2SO4��������Ϻ�������Һ����������________(����ڡ�����С�ڡ����ڡ�)40%������������ϣ���Ϻ���Һ����������________(����ڡ�����С�ڡ����ڡ�)40%��
��2����֪98%��ŨH2SO4�����ʵ���Ũ��Ϊ18.4 mol��L��1�����ж�49%��H2SO4�����ʵ���Ũ��________(����ڡ�����С�ڡ����ڡ�)9.2 mol��L��1��
��3����һ���¶Ⱥ�ѹǿ�£�1���X2(g)��3���Y2(g)��������2���Z(g)����Z����Ļ�ѧʽ��________ ��
��4���ڱ�״���£�CO��CO2�Ļ����������Ϊ36 g�����Ϊ22.4 L����CO��ռ�������__________ L��������________ g��
�ο��𰸣���1������ ���� ��2��С�ڣ�3��XY3 ��4��1
���������
�����������1����ԭ��������Ϊm��30%��H2SO4����Ϊ����0.4m��50%��H2SO4���ʵ�����Ϊ0.5m����Ϻ���������仯���������䣬����w��H2SO4��=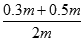 ��100%=40%������������ϣ�������ֱ�ΪVml��30%��H2SO4��Һ�ܶ�Ϊ��1��50%��H2SO4��Һ�ܶ�Ϊ��2�����Ϻ���Һ����������Ϊw��H2SO4��=
��100%=40%������������ϣ�������ֱ�ΪVml��30%��H2SO4��Һ�ܶ�Ϊ��1��50%��H2SO4��Һ�ܶ�Ϊ��2�����Ϻ���Һ����������Ϊw��H2SO4��=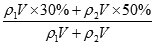 ��100%���������Ũ��Խ���ܶ�Խ�����1����2����w��H2SO4����40%����2��������c=
��100%���������Ũ��Խ���ܶ�Խ�����1����2����w��H2SO4����40%����2��������c=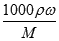 ���㣬��98%��ŨH2SO4���ܶ�Ϊx��49%��H2SO4��Һ���ܶ�Ϊy�����ʵ���Ũ��Ϊc����
���㣬��98%��ŨH2SO4���ܶ�Ϊx��49%��H2SO4��Һ���ܶ�Ϊy�����ʵ���Ũ��Ϊc����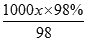 =18.4��
=18.4��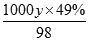 =c�����ԣ�
=c�����ԣ� =
=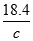 ���������Ũ��Խ���ܶ�Խ����x��y����c��9.2mol/L����3�����ݰ����ӵ����ɿ�֪��1molX2��3molY2��������2mol�����廯������Ը���ԭ���غ㼴�����غ㶨�ɿ�֪���û�����Ļ�ѧʽ��XY3����4����CO�����ʵ���ΪXmol��CO2�����ʵ���ΪYmol����28X+44Y=36��X+Y=1�����X=Y=0.5����CO�����=0.5mol��22.4L/mol=11.2L ,����Ϊ=0.5mol��28g/mol=14g��
���������Ũ��Խ���ܶ�Խ����x��y����c��9.2mol/L����3�����ݰ����ӵ����ɿ�֪��1molX2��3molY2��������2mol�����廯������Ը���ԭ���غ㼴�����غ㶨�ɿ�֪���û�����Ļ�ѧʽ��XY3����4����CO�����ʵ���ΪXmol��CO2�����ʵ���ΪYmol����28X+44Y=36��X+Y=1�����X=Y=0.5����CO�����=0.5mol��22.4L/mol=11.2L ,����Ϊ=0.5mol��28g/mol=14g��
���㣺��ҺŨ�ȵļ���
�����Ѷȣ�һ��
3��ѡ���� �±�Ϊ������Һ�������������������ʵ���Ũ�ȵ���ֵ�����ݱ��������ж�������Һ���ܶ���С����
��Һ
| KOH
| HNO3
| CH3COOH
| HCl
|
������������w(%)
| 56
| 63
| 60
| 36.5
|
���ʵ���Ũ��c(mol��L��1)
| 14.3
| 13.8
| 10.6
| 11.8
?
A.HCl??????????B��HNO3?????????C��CH3COOH?????????D��KOH
�ο��𰸣�C
�������������Һ���ܶ�Ϊ��(g/L)�����ΪV(L)�����ʵ�Ħ������ΪM(g��mol��1)����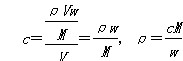 ������ɼ����CH3COOH��Һ���ܶ���С�� ������ɼ����CH3COOH��Һ���ܶ���С��
�����Ѷȣ�һ��
4��ѡ���� 2008��5���ҹ��봨���������ֺ���������������������Ա��Ϊ����0.01 mol/L��KMnO4����Һ�����в�������������ҺŨ��ƫ�ߵ���
A��ȡKMnO4��Ʒʱ�����ڱ���մ�˵�����ˮ
B���ܽ����ʱ��Һ��ɽ�
C������ʱ��������ƿ�̶���
D��ҡ�Ⱥ��Һ���½����ټ�ˮ���̶���
�ο��𰸣�C
���������
���������A��KMnO4��Ʒ����մˮ����ʹ���ʵ������٣�Ũ�ȱ�С��B���ܽ����ʱ��Һ��ɽ���Ҳ������ʼ��٣�Ũ�ȱ�С��D��ҡ�Ⱥ��Һ���½����ټ�ˮ���̶��ߣ������Һ������Ũ�ȱ�С��C��ݸ�������ƿ�̶��ߣ�����Һ�����С��Ũ��ƫ��ѡD��
�����Ѷȣ�һ��
5�������� (1)��Ҫ����100mL 0��1mol��L��Na2SO4��Һ�������Na2SO4������Ϊ���٣�
(2)��2240mL(��״��)����ȫ����ˮ���10 0mL��Һ����ˮ��NH3�����ʵ���Ũ�� (������NH3��H2O�ķ�Ӧ)�� 0mL��Һ����ˮ��NH3�����ʵ���Ũ�� (������NH3��H2O�ķ�Ӧ)��
(3)����һ����о���ѧϰ�У�����Ҫ��ȡ2240mL(��״��)������������Ҫ�Ȼ�淋�������
�ο��𰸣�(1)1.4g(��1.42gҲ����)??��2��1mol�qL<
�����������
�����Ѷȣ�һ��
|