��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�Ȼ�þ��Һ���ܶ�Ϊ1.18g/cm3������þ���ӵ���������Ϊ5.1%��300mL����Һ�������ӵ����ʵ���Ϊ
A��0.37mol
B��0.63mol
C��0.74mol
D��1.5mol
�ο��𰸣�D
���������
����������Ȼ�þ��Һ������Ϊ��1.18g?cm-3��300mL=354g��þ���ӵ�����Ϊ��354g��5.1%=3.54��5.1g��þ���ӵ����ʵ���Ϊ��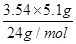 =0.75mol�����ݵ���غ��Ȼ�þ��Һ��n��Cl-��=2n��Mg2+��=2��0.75mol=1.5mol����D��ȷ��
=0.75mol�����ݵ���غ��Ȼ�þ��Һ��n��Cl-��=2n��Mg2+��=2��0.75mol=1.5mol����D��ȷ��
�����Ѷȣ�һ��
2��ѡ���� m g �����뺬��H2SO4��CuSO4 ��Һ��ȫ��Ӧ�õ�m g ͭ������뷴Ӧ��CuSO4��H2SO4�����ʵ���֮��Ϊ
A��7:1
B��1:7
C��7:8
D��8:7
�ο��𰸣�A
���������
�������������뷴Ӧ��CuSO4��H2SO4�����ʵ����ֱ���x��y����������ͭ��������ǿ������ģ����������Ⱥ�����ͭ��Ӧ��Ȼ���ٺ����ᷴӦ������ʽ�ֱ���CuSO4��Fe=FeSO4��Cu��H2SO4��Fe=FeSO4��H2�������Ը��ݷ���ʽ��֪����x��y����56��m��x��64��m�����x�Uy��7:1����ѡA��
�������ڸ��ݷ���ʽ�����йؼ���ʱ���ؼ���ȷ�жϳ���Ӧ�Ĺ��̣�д����Ӧ�ķ���ʽ��Ȼ�����������ó���ϵʽ���ɣ�����Ҳ�������ݵ�ʧ�����غ�����������ʽ���м��㡣
�����Ѷȣ�һ��
3��ѡ���� �����£�2L���ʵ���Ũ��Ϊ0.5mol��L-1K2SO4��Һ����
A��0.5mol��SO42-
B��0.5mol��K+
C��1.0mol��K+
D��96g��SO42-
�ο��𰸣�D
���������
�������������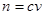 ��K2SO4Ϊ1mol��SO42-Ϊ1mol��K+ Ϊ2mol��SO42-����Ϊ96g����D����ȷ��
��K2SO4Ϊ1mol��SO42-Ϊ1mol��K+ Ϊ2mol��SO42-����Ϊ96g����D����ȷ��
���㣺���⿼�����ʵ���Ũ�� ��
�����Ѷȣ�һ��
4��ѡ���� �����ܱ������зֱ����N2��H2��O2�������壬���¸��������������ȷ����
A�������ǵ�������¶ȡ�ѹǿ����ͬʱ������������ܶȦ�(H2)>��(N2)>��(O2)
B�������ǵ��¶Ⱥ��ܶȶ���ͬʱ�����������ѹǿp(H2)>p(N2)>p(O2)
C�������ǵ��������¶ȡ�ѹǿ����ͬʱ��������������V(O2)>V(N2)>V(H2)
D�������ǵ�ѹǿ��������¶Ⱦ���ͬʱ���������������m(H2)>m(N2)>m(O2)
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
5�������� ȡ1��43g Na2CO3��10H2O����ˮ���100ml��Һ����
��1��Na2CO3���ʵ���Ũ��
��2��Na+ ���ʵ���Ũ��
��3��ȡ��20ml����Һ������ˮϡ�ͣ�ʹNa2CO3��Һ���ʵ���Ũ�ȱ�Ϊ0��004mol/L�����������ˮ���������ϡ��ʱ������Һ�����Ӱ����Բ��ƣ�
�ο��𰸣���1��0��05mol/l��
��2��0��1mol/L
���������
�����Ѷȣ�һ��