微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 早在1807年化学家戴维用电解熔融氢氧化钠制得钠,反应原理为:4NaOH(熔融) 4Na+2H2O+O2↑。后来盖・吕萨克用铁与熔融?氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是
4Na+2H2O+O2↑。后来盖・吕萨克用铁与熔融?氢氧化钠作用也制得钠,反应原理为:3Fe+4NaOH=Fe3O4+4Na↑+2H2↑。下列有关说法不正确的是

A.电解熔融氢氧化钠制钠,阴极发生电极反应为:Na++e-=Na
B.盖・吕萨克法制钠原理是嫡的增加带动了反应的进行
C.若戴维法与盖・吕萨克法制得等量的钠,则两反应中转移的电子总数比为1:1
D.目前工业上常用电解熔融氯化钠法制钠(如图),电解槽中石墨极为阳极,铁为阴极
参考答案:C
本题解析:
试题分析:A、电解池中阴极得到电子发生还原反应,则电解熔融氢氧化钠制钠,阴极发生电极反应为Na++e-=Na,A正确;B、根据反应式3Fe+4NaOH=Fe3O4+4Na↑+2H2↑可知,该反应是熵值增加的反应,因此盖・吕萨克法制钠原理是嫡的增加带动了反应的进行,B正确;C、根据反应方程式可知,若制得1mol钠,则戴维法与盖・吕萨克法中转移电子的物质的量是1mol、2mol,C不正确;D、电解池中阳极失去电子,阴极得到电子,因此用电解熔融氯化钠法制钠时,电解槽中石墨极为阳极,铁为阴极,则D正确,答
本题难度:一般
2、选择题 用铂电极电解CuSO4溶液,当Cu2+浓度降至一半时停止通电,若使CuSO4溶液恢复到原浓度,应加入的物质是()
A.CuSO4
B.CuO
C.Cu(OH)2
D.CuSO4・H2O
参考答案:B
本题解析:发生的电解池反应为2CuSO4+2H2O 2Cu↓+O2↑+2H2SO4,电解中CuSO4溶液每损失2个Cu原子,就损失2个O原子,相当于损失CuO。为了使CuSO4溶液恢复原浓度,显然应加入CuO。
2Cu↓+O2↑+2H2SO4,电解中CuSO4溶液每损失2个Cu原子,就损失2个O原子,相当于损失CuO。为了使CuSO4溶液恢复原浓度,显然应加入CuO。
本题难度:简单
3、填空题 (1)?电池反应通常是放热反应,下列反应在理论上可设计成原电池的化学反应是____________?(填序号)。此类反应具备的条件是①__________反应,②_________反应。 ??
A.C(s)+H2O(g)==CO(g)+H2(g):△H>0??
B.Ba(OH)2・8H2O(s)+2NH4Cl(s)==BaCl2(aq)+2NH3・H2O( ?)+8H2O(
?)+8H2O(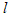 ?)△H>0 ??
?)△H>0 ??
C.CaC2(s)+2?H2O( )==Ca(OH)2(s)+C2H2(g);△H<0 ??
)==Ca(OH)2(s)+C2H2(g);△H<0 ??
D.CH4(g)+2O2(g)==CO2(g)+2H2O(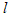 ?):△H<0
?):△H<0
(2)?以KOH溶液为电解质溶液,依据(I)所选反应设计一个电池。其负极反应为:________。
(3)?电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则 ??
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是______?。??
②若X、Y分别为石墨和铁,a仍为饱和的NaCI溶液,则电解过程中生成的白色固体露置在空气中,可观察到的现象是____________。 ???
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为___________。通电一段时间后,向所得溶液中加入0.05?mol?Cu(OH)2,恰好恢复电解前的浓度和PH,则电解过程中电子转移的物质的量为______________mol。
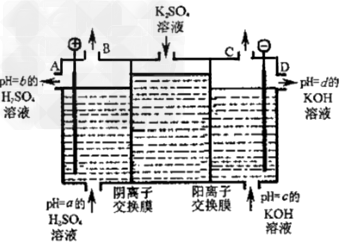
(4)利用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
①?该电解槽的阳极反应式为___________,通过阴离子交换膜的离子数___________(填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②?图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为___________?;
③?电解一段时间后,B口与C口产生气体的质量比为__________。
参考答案:(1)D、放热、氧化还原
(2)CH4-8e-+10O
本题解析:
本题难度:一般
4、填空题 (1)氢氧燃料电池以熔融态的碳酸盐为电解质,其中CO2会参与电极反应。
工作时负极的电极反应为 ;
;
正极的电极反应为_____________ ;向电池负极移动的离子是________________。
(2)用下图所示装置精炼粗铜,则X电极应为__________ ,Y电极应为_________ 。若X、Y电极均为碳棒,则发生反应的化学方程式为____________ ,反应一段时间后,与电源正极相连的电极附近溶液的pH ____________(填“增大”、“减小”或“不变”)。

(3)工业上处理含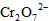 的酸性工业废水的方法如下:
的酸性工业废水的方法如下:
a. 向工业废水中加入适量的NaCl,搅拌均匀;
b. 用Fe作电极,电解一段时间,生成Cr(OH)3和Fe(OH)3沉淀;
c. 过滤,废水达到排放标准。
①电解时,阴极的电极反应式为__________ ;阳极的电极反应式为___________ ;
②能否将Fe电极换成石墨电极 _________(填“能”或“不能”),原因是____________ 。
参考答案:(1)![]() 本题解析:
本题解析:
本题难度:一般
5、填空题 (16分)四种短周期元素A、B、C、D的性质或结构信息如下。
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题。
(1)①C元素在周期表中的位置?????????, 请写出BC2分子的电子式____________。
②A元素的单质与物质甲发生反应的离子方程式___________________。
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式。负极__________;正极(2)A所在周期中, E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,

X、Y都是惰性电极,实验开始时,同时在两边各滴入
几滴酚酞试液,则
①电解池中Y极上的电极反应式????????????????。
检验Y电极反应产物的方法是???????????
②电解一段时间后,若阴极收集到112ml标准状况下的气体,
此时电解液的PH为??????(假设电解液的体积保持不变,常温下)
参考答案:16分,每空2分)
(1)①第2周期ⅥA族?;??
本题解析:略
本题难度:一般