微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 由铜、锌和稀盐酸组成的原电池中,铜是________极,发生________反应,电极反应式是________;锌是________极,发生________反应,电极反应式是________。
参考答案:正还原? 2H++2e-=H2↑?负氧化? Zn-2e-=Z
本题解析:考查原电池的判断及电极反应式的书写。在原电池较活泼的金属作负极,失去电子,被氧化发生氧化反应。所失去的电子经导线传递到正极,所以溶液中到阳离子向正极移动,正极得到,发生还原反应。锌比铜活泼,锌是负极,失去电子。铜是正极,溶液中的氢离子在正极得到电子生成氢气。
本题难度:简单
2、填空题 请回答下列化学有关问题:
(1)现代工业将煤汽化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的用途。
①已知:2C(s)+O2(g)=2CO(g);ΔH1 ,? 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH=???????。(用含ΔH1、ΔH2的代数式表示)
CO(g)+H2(g);ΔH=???????。(用含ΔH1、ΔH2的代数式表示)
②CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol?CO和2mol?H2的混合气体,控温,进行实验测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol?CO和2mol?H2的混合气体,控温,进行实验测得相关数据如下图1和图2。
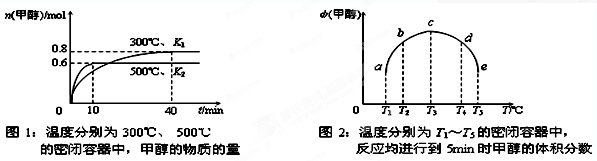
a. 该反应的ΔH3????0(选填“<”、“>”或“=”,下同), K1????K2。??
b. 将容器d中的平衡状态转变到容器c中的平衡状态,可采取的措施有??????????。
(2)煤汽化后的煤渣可提炼重金属。右图为某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液的pH,金属阳离子浓度变化情况。据图分析:
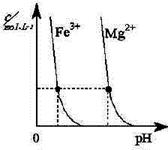
该温度下,溶度积常数的关系为:Ksp[ Fe(OH)3]____Ksp[Mg(OH)2]
(填:>、=、<);如果在新生成的Mg(OH)2浊液中滴入足量的Fe3+,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是???????????
参考答案:(1)(7分)? ① (ΔH1-ΔH
本题解析:(1)①根据盖斯定律可知,(①-②)÷2即得到C(s)+H2O(g)  CO(g)+H2(g),所以ΔH= (ΔH1-ΔH2)/2。
CO(g)+H2(g),所以ΔH= (ΔH1-ΔH2)/2。
②根据图像可知,温度高,平衡时甲醇的低,说明升高温度,平衡溴逆反应方向移动,
本题难度:一般
3、选择题 某原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu ,此反应原电池的正确组成是[???? ]
正极
负极
电解质溶液
A.
Cu
Zn
HCl
B.
Zn
Cu
CuS04
C.
Cu
Zn
CuS04
D.
Cu
Zn
ZnCl2
参考答案:C
本题解析:
本题难度:简单
4、选择题 人们利用原电池原理,制作了多种电池,如电子计算机所用钮扣电池就是其中一种.它的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应是:Zn+2OH--2e-===ZnO+H2O;Ag2O+H2O+2e-===2Ag+2OH-.下列判断正确的是 [???? ]
A.锌为正极,Ag2O为负极
B.锌为负极,Ag2O为正极
C.原电池工作时,负极区溶液pH减小
D.原电池工作时,负极区溶液pH增大
参考答案:BC
本题解析:
本题难度:一般
5、填空题 23.(12分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上合成甲醇的反应原理为:CO(g) + 2H2(g)  CH3OH(g) ΔH;
CH3OH(g) ΔH;
下表所列数据是该反应在不同温度下的化学平衡常数(K)。
温度
| 250℃
| 300℃
| 350℃
|
K
| 2.041
| 0.270
| 0.012
①根据表中数据可判断ΔH 0 (填“>”、“=”或“<”)。
②在300℃时,将2 mol CO、3 mol H2和2 mol CH3OH充入容积为1L的密闭容器中,此时反应将 (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”)。
(2)以甲醇、氧气为原料,KOH溶液作为电解质构成燃料电池总反应为:2CH3OH+3O2+4OH-=2CO32-+6H2O,则负极的电极反应式为: ,随着反应的不断进行溶液的pH (填“增大”“减小”或“不变”)。
(3)如果以该燃料电池为电源,石墨作两极电解饱和食盐水,则该电解过程中阳极的电极反应式为: ;如果电解一段时间后NaCl溶液的体积为1L,溶液的pH为12(25℃下测定),则理论上消耗氧气的体积为 mL(标况下)。
参考答案:(1)①< ②向正反应方向进行
(2) CH
本题解析:
试题分析:根据所给表格可知随着温度的升高,K逐渐减小,得到该反应为放热反应,因而ΔH<0;在300℃时,将2 mol CO、3 mol H2和2 mol CH3OH充入容积为1L的密闭容器中,CO有剩余,反应物的浓度增大,平衡向正反应方向移动;将总反应分解得负极的电极反应CH3OH+ 8OH―-6e―= CO32―+6H2O;随着反应的进行,H+逐渐产生,所以pH减小;电解饱和食盐水,阳极生成了氯气,电极反应:2Cl―-2e―=Cl2↑;pH=12说明c(OH-)=0.01mol/L;根据电荷守恒,n(O2)=0.0025mol,V=0.056L=56ml
考点:化学平衡及相关计算
点评:本题做题的关键是掌握平衡移动的原理,将燃料电池的知识与平衡移动相联系,综合性较强。
本题难度:困难
|