微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 [三选一―选修3:物质结构与性质]
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。 ?
(1)①H、C、N、O四种元素的电负性由小到大的顺序为?____________。
②下列叙述不正确的是____________。(填字母) ??????
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水 ??????
B.HCHO和CO2分子中的中心原子均采用sp2杂化 ??????
C.C6H6分子中含有6个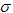 键和1个大
键和1个大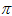 键,C2H2是非极性分子 ??????
键,C2H2是非极性分子 ??????
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低?
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式____________。
(2)?Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是_____________??
②六氰合亚铁离子[Fe(CN)6]4?-中不存在_______________。
A、共价键???B、非极性键???C、配位键???D、σ键???E、π键
写出一种与?CN-??互为等电子体的单质分子式______________。
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于_________?区。
(4)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:???
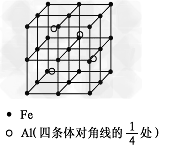
①?确定该合金的化学式__________?。
②?若晶体的密度=ρ?g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为_______________cm。
2、选择题 目前,科学家拟合成一种“二重构造”的球形分子,即把足球型的C60分子融进到Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列说法正确的是( )
A.它是由两种单质组成的混合物
B.它是一种碳酸盐
C.它是一种新型化合物
D.它是一种离子晶体
3、选择题 根据下表中的数据,结合学过的化学知识,判断下列说法正确的是
物质
| NaCl
| MgCl2
| AlCl3
| SiCl4
|
沸点/℃
| 1465
| 1412
| 181(升华)
| 57.6
A.以上四种物质中,只有SiCl4是共价化合物
B.若上述数据变化规律具有普遍性,则可预测:LiCl 的沸点大于BCl3的沸点
C.因为AlCl3的沸点低,所以工业上可用电解熔融AlCl3制备Al
D.据上述数据,可判断NaCl、MgCl2为分子晶体
4、填空题 某离子晶体晶胞结构如图所示,x位于立方体的顶点,Y位于立方体中心.试分析:
该晶体的化学式为______.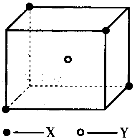
5、选择题 氮氧化铝(AlON)属原子晶体,是一种超强透明材料,下列描述错误的是(???)
A.AlON和石英的化学键类型相同
B.AlON和石英晶体类型相同
C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同
D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同
|