微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)下图中的实验装置可用于制取乙炔。请填空:
 ?
?
(1)图中,A管的作用是?????????????????????????????。
制取乙炔的化学方程式是????????????????????????。
(2)乙炔通入KMnO4酸性溶液中观察到的现象是????????,乙炔发生了?????反应。
(3)乙炔通入溴的CCl4溶液中观察到的现象是??????????,乙炔发生了???????反应。
(4)为了安全,点燃乙炔前应???????????????,乙炔燃烧时的实验现象是???????????????????????????????????????????。
参考答案:(1)调节水面高度以控制反应的发生与停止;CaC2+2H2O
本题解析:(1)因为电石与水很剧烈,反应不易控制,所以通过调节水面高度以控制反应的发生与停止,方程式为CaC2+2H2O →C2H2↑+ Ca(OH)2。
(2)乙炔中含有碳碳三键,容易被氧化,所以乙炔可以使酸性高锰酸钾溶液褪色。
(3)同样因为乙炔中含有碳碳三键,容易发生加成反应,所以乙炔可以使溴的CCl4溶液褪色。
(4)乙炔实验可燃性气体,点燃前需要检验其纯度。防止燃烧时爆炸。乙炔中含碳量很高,燃烧时火焰明亮并伴有浓烈黑烟。
本题难度:简单
2、选择题 下列气体的收集用错装置的是[???? ]
A.Cl2的收集???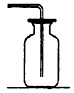
B.NO的收集???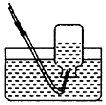 ?????
?????
C.NH3的收集??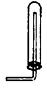
D.NO的收集? 
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列气体中,不能用排空气收集的是
A.NO
B.NO2
C.CO2
D.H2
参考答案:A
本题解析:NO极易被氧气氧化生成NO2,所以不能用排气法收集,而是用排水法收集。其余都可以用排气法收集,所以答案是A。
本题难度:一般
4、填空题 (12分)自洁面料就是在普通的面料纤维中加入一层薄薄的纳米二氧化钛。含有Fe2O3的钛铁矿(主要成分为FeTiO3,Ti的最高价为 +4)制取纳米级TiO2的流程如下:
+4)制取纳米级TiO2的流程如下:
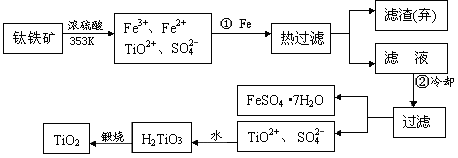
(1)步骤①发生的主要反应是_____????_____?????????_______(用离子方程式表示)
(2)上述制备二氧化钛的过程中,可以利用的副产物是______________;考虑成本和废物综合利用因素,废液中应加入___________________处理。
(3)由金红石制备单质钛,涉及到的步骤为:
TiO2 TiCl4
TiCl4 Ti?
Ti?
已知:①C(s)+O2(g)=CO2(g)?△H=?-393.5kJ・mol-1
②2CO(g)+O2(g)=2CO2(g)?△H=?-566.0kJ・mol-1
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g)?△H=?+141.0kJ・mol-1
则TiO2(s)+ 2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H=____________ kJ・mol-1
反应TiCl4+2Mg =?2MgCl2+Ti 在氩气氛中进行的理由是________________________。
(4)TiO2是白色粉末,不溶于水,也不溶于酸,但能溶于氢氟酸和热的浓硫酸中。请写出TiO2与硫酸反应的方程式?????????????????????????????????????
参考答案:(1)2Fe3+ + Fe=3 本题解析:略
本题解析:略
本题难度:一般
5、填空题 (Ⅰ)某化学兴趣小组的同学得上用下 图所示实验装置进行实验(图中a、b、c表示止水夹)。
图所示实验装置进行实验(图中a、b、c表示止水夹)。
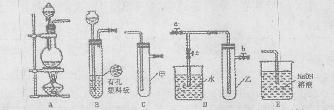
(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱。
①选择合理的装置连接:???????????→????????????→??????????(填字母编号)。
②选择所需的试剂:??????????(填字母编号)。
a.固体氯化钠??? b.固体二氧化锰??? c.浓硫酸
d.浓盐酸??????? e.稀盐酸????????? f.溴化钠溶液
③实验现象及结论:?????????。
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4・7H2O晶体,设计实验流程如下:

已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
M(OH)n
| Ksp[来
| pH
|
开始沉淀
| 沉淀完全
|
Al(OH)3
| 1.9×10-23
| 3.43
| 4.19
|
Fe(OH)3
| 3.8×10-38
| 2.53
| 2.94
|
Ni(OH)2
| 1.6×10-14
| 7.60
| 9.75
???回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀I是???????沉淀II是????????(填化学式),pH1???????????pH2(填“>”、“<”或“=”);
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为???????????。
(3)“调节pH为2-3”的目的是???????;
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料――NiOOH。该反应的离子方程式是??????????????。
参考答案: 本题解析:略 本题解析:略
本题难度:一般
|