微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (15分)图1是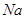 、
、 、
、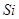 、
、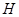 、
、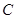 、
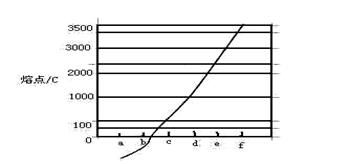
、 等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。 (1)图中d的单质对应元素原子的电子排布式是????????????????????
等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。 (1)图中d的单质对应元素原子的电子排布式是????????????????????
(2)单质a、b、f对应的元素以原子个数比1:1:1形成的分子中含???个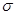 键,???个
键,???个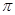 键。
键。
(3)a与b的元素形成的10个电子中性分子X的空间构型为???????;将X溶于水后的溶液滴入到含d元素高价离子的溶液中至过量,生成d元素的离子化学式为????,其中X与d 高价离子之间以??????键相结合。
(4)图2是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:?????????????????????????????????????????????????????????????????????。
(5)图中C单质的晶体堆积方式类型是?????,这种堆积方式晶胞中原子的配位数为??????。
?
 ??
??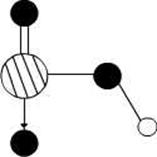
图1???????????????????????????????????图2
参考答案:(1) 本题解析:(1)c、d均是热和电的良导体。且d的熔点高于c的,所以c是钠,d是铜,根据构造原理可知电子排布为
本题解析:(1)c、d均是热和电的良导体。且d的熔点高于c的,所以c是钠,d是铜,根据构造原理可知电子排布为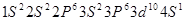 。
。
(2)根据熔点高低可判断,a是氢气,b是氮气,e是硅,f是金刚石。a、b、f对应的元素以原子个数比1:1:1形成的分子是HCN,其中氢和碳是单键,碳和氮是三键,所以含有的 本题难度:一般
本题难度:一般
2、填空题 用VSEPR理论判断
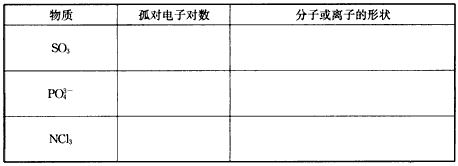
参考答案:![]() 本题解析:
本题解析:
本题难度:一般
3、简答题 A、B、C、D、E五种元素中,A原子第三能层轨道上成对电子数等于未成对电子数,B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同,C的价电子排布式为nsnnpn+2,D的核电荷数是A与C的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)A的最高价氧化物的化学式为______,中心原子的VSEPR构型为______.
(2)AC2与BC2分子的立体结构分别是______和______,相同条件下两者在水中的溶解度较大的是______(写分子式),理由是______.
(3)D的元素符号是______,它的价电子排布式为______,在形成化合物时它的最高化合价为______.
(4)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键______.
参考答案:A原子第三能层轨道上成对电子数等于未成对电子数,价电子排布应
本题解析:
本题难度:一般
4、选择题 下列说法正确的是(??)
A.某晶体固态不导电,水溶液能导电说明该晶体是离子晶体
B.原子晶体的原子间只存在共价键,而分子晶体内只存在范德华力。
C.区分晶体和非晶体最科学的方法是对固体进行X-射线衍射实验
D.任何晶体中,若含有阳离子也一定含有阴离子
参考答案:C
本题解析:考查晶体的性质和判断。区分离子晶体还是分子晶体可以通过熔融时能否导电来验证。分子晶体在熔融时不能导电,A不正确。在分子晶体内还可以存在共价键,B不正确。D不正确,例如金属晶体中存在阳离子,但没有阴离子。所以正确的答案是C。
本题难度:简单
5、选择题 下列描述中正确的是( )
A.CS2分子的立体结构为V形
B.SiF4和SO32-的中心原子均为sp2杂化
C.SF6中有6对完全相同的成键电子对
D.ClO3-的空间构型为平面三角形
参考答案:C
本题解析:
本题难度:一般