微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知2X2(g)+Y2(g)?2Z(g)△H=-akJ?mol-1(a>0),在一个容积固定的容器中加入2mol X2和1mol Y2,在500℃时充分反应达平衡后Z的浓度为W mol?L-1,放出热量bkJ.
(1)此反应平衡常数表达式为______;若将温度降低到300℃,则反应平衡常数将______(填增大、减少或不变).
(2)若原来容器中只加入2mol Z,500℃充分反应达平衡后,吸收热量ckJ,则Z浓度______W mol?L-1(填“>”、“<”或“=”),a、b、c之间满足关系______(用代数式表示).
(3)若将上述容器改为恒压容器(反应器开始体积相同),相同温度下起始加入2molX2和1molY2达到平衡后,Y2的转化率将______(填“变大”、“变小”或“不变”).
参考答案:(1)化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生
本题解析:
本题难度:简单
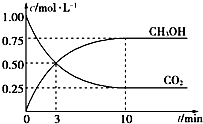
2、选择题 已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.一定条件下,向体积为1L的密闭容器中充入1mol?CO2和3mol?H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示.下列叙述中正确的是( )
A.欲增大平衡状态时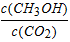 的比值,可采用升高温度的方法
的比值,可采用升高温度的方法
B.3?min时,CO2的消耗速率等于CH3OH的生成速率,且二者浓度相同
C.欲提高H2的平衡转化率只能加压减小反应容器的体积
D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075?mol?L-1?min-1
参考答案:B
本题解析:
本题难度:简单
3、简答题 合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ/mol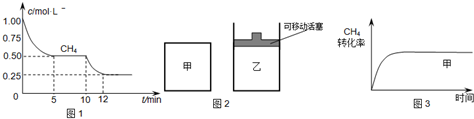
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为______;10min时,改变的外界条件可能是______.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)反应CO(g)+H2O(g)?CO2(g)+H2(g)800℃时,反应的化学平衡常数K=1.0.
①某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2
0.5mol
8.5mol
2.0mol
2.0mol
此时反应中正、逆反应速率的关系式是______(填代号).
a.v(正)>v(逆)b.v(正)<v(逆)c.v(正)=v(逆)d.无法判断
②800℃时,向体积为2L的密闭容器中充入2molCO和4molH2O,求达到平衡时CO的转化率.
参考答案:(1)由图可知,由图可知,在5~10分钟、12分钟后,甲烷浓
本题解析:
本题难度:简单
4、选择题 下图中的两条曲线分别表示200℃和300℃时,有反应A(g)+B(g)

C(g),△H体系中B的百分含量和时间t的关系,下列对△H的数值和表示300℃时的变化曲线的说法正确的是( )
A.△H<0,R曲线
B.△H>0,R曲线
C.△H<0,S曲线
D.△H>0,S曲线

参考答案:A
本题解析:
本题难度:一般
5、填空题 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:

(1)该反应所用的催化剂是___________(填写化合物名称),该反应450℃时的平衡常数________500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是____________。
(3)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molSO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则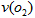 =___________mol/L・min:若继续通入0.20mol SO2和0.10mol O2,则平衡__________移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,_______mol< =___________mol/L・min:若继续通入0.20mol SO2和0.10mol O2,则平衡__________移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,_______mol<
n(SO3)<________mol
参考答案:(1)五氧化二钒(V2O5);大于
(2)在450℃时
本题解析:
本题难度:一般
|