微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 Mg及其化合物可以发生如下转化(部分反应物、生成物或水已略去),已知X、Y、Z为气态单质,B常温下为液态,D为化合物,它的焰色反应为黄色,C和G混合冒白烟并生成A
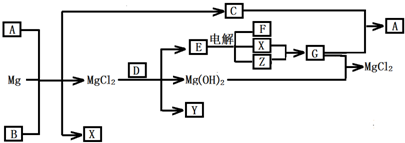
(1)写出下列物质的化学式:A______?Y______
(2)写出C的电子式______
(3)写出MgCl2与D反应的化学方程式______
(4)请用电离或水解平衡解释A+B+Mg→C+X+MgCl2的原因______.
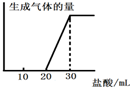
(5)将1molCO2通入1L溶质为F的溶液中,充分反应后,再向混合液中逐滴滴加盐酸,所加盐酸的体积与生成的气体的关系如图所示则原F溶液的浓度为______mol/L.
2、填空题 (9分)有一包白色粉末状混合物,可能含有Na2CO3、NaCl、CaCO3、CuSO4、KCl、Na2SO4、MgCl2、KNO3中的某几种,现进行如下实验:
①将混合物溶于水,得到无色透明溶液。
②取少量上述溶液两份,其中一份加入BaCl2溶液,立即产生白色沉淀,再加上稀硝酸,沉淀不溶解,在另一份中加入NaOH溶液,也产生白色沉淀。
根据上述实验现象回答:
(1)原混合物中肯定没有__________________________。
(2)原混合物中肯定有____________________________。
(3)不能确定是否含有____________________________。
3、填空题 (12分)X、Y、Z、W均为含有10电子的微粒,其中Z、Y、Z为分子,W为离子,且X与Z分子中含有的共用电子对数之比为3:4。
请回答:
(1)X的电子式????????;若实验室用如图所示装置制取X,则制取X的化学反应方程式为??????????。
(2)已知:W+X+H2O一白色沉淀,为进一步确定W,进行如下实验,请补全实验操作、现象和结论:取上述白色沉淀少量置于试管中,???????。
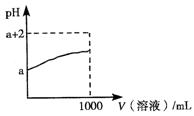
(3)常温下,取10 mL pH=a的Y的稀溶液,加水稀释时pH随溶液体积的变化如图所示,则Y的化学式为??????????,下列叙述正确的是????(选填字母)。

a.Y的水溶液可用作刻蚀玻璃
b.相同温度时与相同浓度的盐酸比较,Y的水溶液的导电能力弱
c.稀释后,阴离子的物质的量浓度:之和增大
(4)分子中所含菜元素对应的单质A及A与B形成的化合物可进行如下转化:
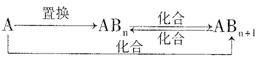
当n=1时,请写出A―ABn的化学方程式???????????(写出一个即可)。
4、简答题 已知金属单质A是生产生活中用量最大的金属.D是难溶于水的白色固体.F为红褐色固体.无色气体甲遇气体丙立即生成红棕色的气体乙(图中部分产物和反应的条件略).
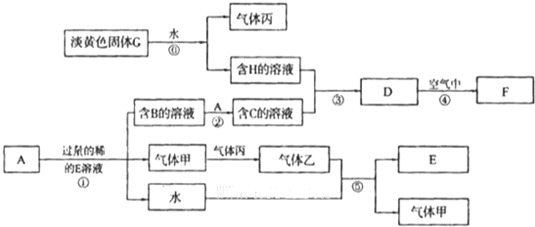
请根据以上信息回答下列问题:
(1)写出下列物质的化学式C______G______.
(2)写出反应①的化学方程式______.反应②的离子方程式______.
(3)反应④整个过程观察到的现象为______.
(4)反应⑤中,若将充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积______.
(5)某种贫血症患者应补充C物质的阳离子.含该离子的药片外表包有一层特殊的糖衣,这层糖衣的作用就是保护该离子不被空气中的氧气氧化.为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴______溶液,溶液显______色,表明该药片已失效.
5、推断题 A、B、C是三种常见短周期元素的单质。常温下D为无色液体,E是一种常见的温室气体。其转化关系如图(反应条件和部分产 物已略去)。试回答:
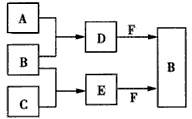
(1)E的电子式是____ 。
(2)单质X和B或D均能反应生成黑色固体Y,Y的化学式是___。
(3)物质Z常用于净化空气、杀菌和水果保鲜等。Z和B的组成元素相同,Z分子中各原子最外层 电子数之和为18。Z和酸性碘化钾溶液反应生成B和碘单质,反应的离子方程式是___。
(4)取0.3 mol F与足量D充分混合后,所得溶液中再通入0.2 mol E充分反应,最后得到的水溶 液中各种离子的浓度由大到小的顺序是(不考虑H+)___。
(5)某课题组利用E催化制甲烷的过程如下。
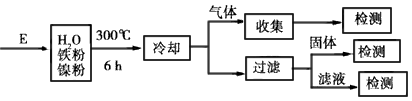
反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。
①写出产生H2的化学方程式___,
②HCOOH是E转化为CH4的中间产物,完成并配平HCOOH转化为CH4的化学反应方程式:
HCOOH+(????? ?) CH4 +H2O
CH4 +H2O