微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 对SO2与CO2说法正确的是[???? ]
A.都是直线形结构
B.中心原子都采取sp杂化轨道
C.S原子和C原子上都没有孤对电子
D.SO2为V形结构, CO2为直线形结构
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列叙述正确的是(?)
A?固体时能导电的晶体一定为金属晶体
B?电负性差值小于1.7的A、B两种元素,组成的化合物也可能为离子化合物
C?某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体
D?由原子构成的晶体均具有熔沸点高、硬度大的特性
参考答案:BC
本题解析:A不正确,例如硅可以导电,但硅是原子晶体。B正确,例如氢化钠等。选项C正确,D不正确,并非所有的原子晶体都具有熔沸点高、硬度大的特性。答案选BC。
本题难度:简单
3、选择题 下面关于晶体的叙述中,错误的是(?? ?)
A.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有6个
C.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
D.金刚石为网状结构,由共价键形成的碳原子环中,最小环上有6个碳原子
参考答案:B
本题解析:
试题分析:B项:氯化钠晶体中,每个Na+周围距离最近且相等的Na+共有12个,故错。故选B。
点评:本题考查的是晶体的相关知识,题目难度不大,注意对基础知识的学习、掌握及应用。
本题难度:一般
4、计算题 (1)中学教材上图示了NaCl的晶体结构,它向三维空间延伸得到完美的晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-。的核间距为a×10-8?cm,计算NiO晶体的密度(已知NiO的相对分子质量为74.7?g/mol)。
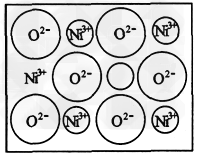
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代;其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。某氧化镍样品组成为Ni0.97O,试计算该晶体中Ni3+与
Ni2+的个数之比。
参考答案:(1)62.0a-3?g/cm3??
(2)N(Ni3
本题解析:
本题难度:一般
5、选择题
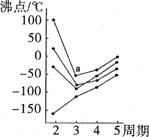
沸点变化,每个小黑点代表一种氢化物,其中a点代表的是
A.NH3
B.H2S
C.SiH4
D.HF
参考答案:B
本题解析:根据a前一物质沸点是100oC,是水,其沸点反常偏高,是因为水分子之间的氢键作用,此元素是氧处于第二周期,故相应第三周期是硫。选B。
本题难度:一般