微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 X元素最高氧化物对应的水化物为H3XO4,则它对应的气态氢化物为[???? ]
A.HX
B.H2X
C.XH4
D.XH3
参考答案:D
本题解析:
本题难度:简单
2、选择题 三氯化氮(NCl3)常温是一种淡黄色液体,其分子结构呈三角锥形,以下关于NCl3的说法中正确的是( )
A.它是一种非极性分子
B.它能以配位键与Cl-结合,生成NCl4-
C.NCl3中N原子采用SP2杂化
D.已知NCl3中N元素为-3价,所以NCl3水解产物为NH3和HClO
参考答案:A、NCl3分子中存在N-Cl极性键,分子呈三角锥形,分子结
本题解析:
本题难度:简单
3、填空题 ( 13分)西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如下表所示:
??分子式
| 结构简式
| 外观
| 熔点
| 溶解性
|
C12H10ClN3O
| 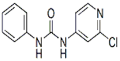
| 白色结晶粉末
| 170~172°C
| 易溶于水
(1)氯元素基态原子核外电子的未成对电子数为?????????。
(2)氯吡苯脲的晶体类型为_______????????,所含第二周期元素第一电离能从大到小的顺序为________________。
(3)氯吡苯脲晶体中,氮原子的杂化轨道类型为______????_。
(4)氯吡苯脲晶体中,微粒间的作用力类型有________????_。
A.离子键B.金属键C.共价键D.配位键E.氢键
(5)氯吡苯脲熔点低,易溶于水的原因分别为_________________________________
________________________________________________________________________。
(6)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。
 异氰酸苯酯???????????????? 2-氯-4-氨基吡啶???????????????氯吡苯脲 异氰酸苯酯???????????????? 2-氯-4-氨基吡啶???????????????氯吡苯脲
反应过程中,每生成1mol氯吡苯脲,断裂_______个σ键、断裂_______个π键
参考答案:(13分)(1)1?(1分)??(2)分子晶体?? N>
本题解析:
试题分析:(1)根据构造原理可知,氯元素基态原子核外电子的排布式是1s22s22p63s23p5,所以未成对电子数为1个。
(2)氯吡苯脲的熔点较低,易溶于水,所以其晶体类型是分子晶体。其中所含第二周期元素分别是C、N、O,非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,稳定性强,所以第一电离能大于氧元素的,即正确的顺序是N>O>C。
(3)根据结构简式可知,2个氮原子全部形成单键,属于sp3杂化。另外一个氮原子形成双键,所以是sp2杂化。
(4)氯吡苯脲
本题难度:一般
4、选择题 下列各项表达中正确的是( )
|