微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 结构简式为
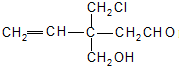
的有机物,不能发生的反应是( )
A.消去反应
B.加成反应
C.酯化反应
D.银镜反应
参考答案:A
本题解析:
本题难度:简单
2、选择题 在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是
A.稀释溶液,水解平衡常数增大
B.通入CO2,平衡向正反应方向移动
C.升高温度,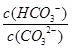 减小
减小
D.加入NaOH固体,溶液pH减小
参考答案:B
本题解析:
试题分析:水解平衡常数只与温度有关,A错;通入CO2,OH-浓度会减小,平衡向正反应方向移动,B对;
升高温度平衡向正向移动,c(HCO3-)增大,c(CO32-)减小,故c(HCO3-)/c(CO32-)增大,C错; NaOH是强碱,加入NaOH固体,溶液的碱性增强,pH增大,D错。
考点:水解平衡的移动和溶液中离子浓度大小变化
本题难度:一般
3、选择题 将下列溶液蒸干、并灼热后,仍能得到原溶质固体的是
A.AlCl3溶液
B.NaAlO2溶液
C.NaHCO3溶液
D.FeSO4溶液
参考答案:B
本题解析:
试题分析:
A、Al3+水解,生成Al(OH)3,同时生成挥发性酸盐酸,最后得到氧化铝固体,故A不合题意;
B、虽然加热时NaAlO2溶液水解生成Al(OH)3,但并未生成挥发性物质,故能得到原物质,符合题意;
C、NaHCO3固体加热时会分解生成碳酸钠,得不到原溶质,故C不合题意;
D、加热时Fe2+水解,硫酸难挥发,但是加热过程中,Fe2+水会被氧化生成Fe2(SO4)3,故不合题意。
考点:盐类的水解的应用
点评:本题考查了盐类的水解,盐溶液的蒸干问题,难度中等。要注意各种物质水解后的产物,以及各物质的特殊性质。
本题难度:一般
4、选择题 常温下,将a mol/L的MOH(可溶性弱碱)与b mol/L盐酸等体积混合,已知相同条件下MOH的电离程度大于M+的水解程度,则下列有关推论不正确的是( )
A.若混合后溶液pH=7,则c(M+)=c(Cl-)
B.若b=2a,则c(Cl-)>c(M+)>c(H+)>c(OH-)
C.若a=2b,则c(M+)>c(Cl-)>c(OH-)>c(H+)
D.若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b
参考答案:B
本题解析:根据溶液的电中性原理可知A项正确;若b=2a,混合后的溶液为等物质的量浓度的MCl和HCl的混合溶液,M+离子部分水解,故c(H+)>c(M+),B项错误;若a=2b,混合后的溶液为等物质的量浓度的MCl和MOH的混合溶液,因MOH的电离程度大于M+的水解程度,故c(OH-)>c(H+),MOH的电离是微弱的,故c(Cl-)>c(OH-),C项正确;若b=a,混合后的溶液为MCl溶液,根据质子守恒可知c(H+)=c(OH-)+c(MOH),D项正确
本题难度:一般
5、选择题 25℃时,将稀氨水逐滴滴加到稀硫酸中,当溶液的pH=7时,下列关系正确的是( )
A.c(NH4+)=c(SO42-)
B.c(NH4+)>c(SO42-)
C.c(NH4+)<c(SO42-)
D.c(NH4+)+c(SO42-)=c(H+)=c(NH4+)
参考答案:B
本题解析:
试题分析:反应后溶液中含有NH4+、SO42?、H+、OH?,根据电荷守恒可得:c(NH4+)+C(H+)=2c(SO42?)+c(OH?),因为pH=7,所以c(H+)=c(OH?),带入电荷守恒关系式可得:c(NH4+)=2c(SO42?),故c(NH4+)>c(SO42?),B项正确。
考点:本题考查电荷守恒、离子浓度关系。
本题难度:一般