微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是
A.正极附近SO42-浓度逐渐增大
B.电子通过导线由铜片流向锌片
C.正极反应式为Zn-2e-=Zn2+
D.该原电池工作过程中电解质溶液的pH增大
参考答案:D
本题解析:负极生成Zn2+,SO42-向负极迁移,A错误;电子通过导线由锌片流向铜片,B错误;C中是负极反应式,C错误;随着硫酸的消耗,溶液的pH增大,D正确。
本题难度:一般
2、选择题 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法正确的是
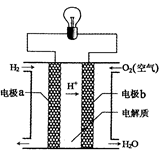
A.该电池的总反应:2H2+O2=2H2O
B.该电池中电极b是负极
C.外电路中电子由电极b通过导线流向电极a
D.该电池工作时电能转化为化学能
参考答案:A
本题解析:试题分析:根据原电池的工作原理可知,负极电极反应式2H2-4 e-=4H+,正极电极反应式为O2+4H++4e-=2H2O,正负极电极反应式相加得电池反应式2H2+O2=2H2O,故A正确;氢氧燃料电池中,通入氢气的一极为电源的负极,所以电极a是负极,故B错误;氢氧燃料电池中,通入氧气的一极为电源的正极,发生还原反应,外电路中电子由电极a通过导线流向电极b,故C错误;氢氧燃料电池中是把化学能转化为电能,故D错误,答案选A。
考点:考查氢氧燃料电池的有关判断
点评:该题以氢氧燃料电池为载体,重点考查学生对原电池原理的熟悉了解程度,实验中等难度的试题。注意电极方程式的书写,电极反应式与电解质溶液的酸碱性有关,电极反应式相加时,得失电子数必须相等等。
本题难度:简单
3、填空题 (9分)水是组成生命体的重要化学物质,有关水的反应有很多。
(1)用电子式表示H2O的形成过程 。
(2)在pH=1的水溶液中,①NH4+、Al3+、Br-、SO42- ② Na+、Fe2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-四组离子中,一定大量共存的是 (填序号)。
(3)在下列反应中,水仅做氧化剂的是 ,水既不做氧化剂又不做还原剂的是 。
A.2F2+2H2O=4HF+O2
B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑
D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数为 。
参考答案: (1)  本题解析:
本题解析:
试题分析:(1)H2O是共价化合物,用电子式表示H2O的形成过程是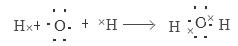 ,(2)在pH=1的酸性水溶液中,①NH4+、Al3+、Br-、SO42-不会发生任何反应,可以大量共存,正确;② 在酸性溶液中H+、Fe2+、NO3-会发生氧化还原反应而不能大量共存,错误;③在酸性溶液中K+、Ba2+、Cl-、NO3-不会发生任何反应,可以大量共存,正确;④在酸性溶液在中H+、HCO3-会发生复分解反应而不能大量共存,错误。因此一定大量共存的是①③;(3)在反应CaH2+2H2O=Ca(OH)2+2H2↑ 和3Fe+4H2O
,(2)在pH=1的酸性水溶液中,①NH4+、Al3+、Br-、SO42-不会发生任何反应,可以大量共存,正确;② 在酸性溶液中H+、Fe2+、NO3-会发生氧化还原反应而不能大量共存,错误;③在酸性溶液中K+、Ba2+、Cl-、NO3-不会发生任何反应,可以大量共存,正确;④在酸性溶液在中H+、HCO3-会发生复分解反应而不能大量共存,错误。因此一定大量共存的是①③;(3)在反应CaH2+2H2O=Ca(OH)2+2H2↑ 和3Fe+4H2O Fe3O4+4H2中水仅做氧化剂;在2Na2O2+2H2O=4NaOH+O2↑中,水既不做氧化剂又不做还原剂;(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,燃料氢气的电极是负极,则负极的电极反应为H2 +2OH - -2e =2H2O;反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,则由于n(H2O)=1800g÷18g/mol=100mol根据原电池的电极反应可知,每产生1mol的水,转移电子2mol,现在产生来 100mol的水,所以电池内转移的电子数为200NA。
Fe3O4+4H2中水仅做氧化剂;在2Na2O2+2H2O=4NaOH+O2↑中,水既不做氧化剂又不做还原剂;(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,燃料氢气的电极是负极,则负极的电极反应为H2 +2OH - -2e =2H2O;反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,则由于n(H2O)=1800g÷18g/mol=100mol根据原电池的电极反应可知,每产生1mol的水,转移电子2mol,现在产生来 100mol的水,所以电池内转移的电子数为200NA。
考点:考查有关水的结构、性质及应用和计算的知识。
本题难度:困难
4、选择题 干电池的总反应方程式为Zn+2NH4+==Zn2++2NH3+H2。下列说法中正确的是
A.锌作正极,发生氧化反应
B.锌作负极,发生氧化反应
C.锌作正极,发生还原反应
D.锌作负极,发生还原反应
参考答案:B
本题解析:在反应总反应方程式为Zn+2NH4+==Zn2++2NH3+H2中,锌元素化合价升高,所以在构成的原电池中,锌为负极,失去电子发生氧化反应;
本题难度:简单
5、选择题 一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通入乙烷和氧气。电极反应式为:C2H6 +180H- -14e-="=" 2C032一+ 12H20; 7H20+7/2 02+14e - ="=140H" -.
下列有关此电池的推断错误的是 ( )
A.在电解质溶液中OH -向正极移动
B.参加反应的02与C2H6的物质的量之比为7:2
C.放电一段时间后,KOH的物质的量浓度将下降
D.通氧气的电极为正极
参考答案:A
本题解析:略
本题难度:一般