��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��ij��˾���������ıʼDZ��������õļ״�ȼ�ϵ�صĹ���ʾ��ͼ���״��ڴ����������ṩ����(H��)�͵��ӣ����Ӿ�����·�����Ӿ��ڵ�·������һ����������Ӧ���õ���ܷ�ӦʽΪ��2CH3OH��3O2===2CO2��4H2O�������йظõ�ص�˵���������(����)

A���ұߵĵ缫Ϊ��صĸ�����b��ͨ����ǿ���
B����ߵĵ缫Ϊ��صĸ�����a��ͨ����Ǽ״�
C����ظ����ķ�ӦʽΪ��2CH3OH��2H2O��12e��===2CO2����12H��
D����������ķ�ӦʽΪ��3O2��12H����12e��===6H2O
2������� ��14�֣��������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2���������ձ�����ӡ�
��1��Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��
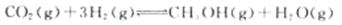
��ͼ��ʾ�÷�Ӧ���й�������������λΪkJ��mol-1���ı仯��

�ٸ÷�Ӧ��????????????������ȡ����ȡ�����Ӧ��
�ڷ�Ӧ��ϵ�м�������Է�Ӧ���Ƿ���Ӱ�죿????����ǡ�����ԭ����???????????????????????????��
��2������6mol CO2��8 mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯��������ͼ��ʾ��ʵ�ߣ���
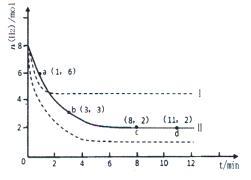
�ٸ������·�Ӧ��ƽ�ⳣ��K=????�����ڴ����ͼ�л���״������ʵ�����ʱ��仯���ߡ�
�ڽ��ı�ijһʵ�������ٽ�������ʵ�飬���H2�����ʵ�����ʱ��仯��ͼ��������ʾ������I��Ӧ��ʵ�������ı���??????�����ߢ��Ӧ��ʵ�������ı���????��
�����д�ʩ����ʹH2ת�����������?????��
A�������¶�
B������He��g����ʹ��ϵѹǿ����
C����H2O��g������ϵ�з������
D���ٳ���3mol CO2��4mol H2
��3���罫CO2��H2��1��4������Ȼ�ϣ����ʵ��������¿��Ƶ�CH4����֪��

д��CO2��g����H2��g����Ӧ����CH4��g����Һ̬ˮ���Ȼ�ѧ����ʽ????��
3������� ��10�֣����ྻ�Ľ���ƬFe��Zn ��A��B �ֱ���Cu�õ���������ں��ʵĵ������Һ�ʵ�鲢��¼��ѹָ����ƶ�����͵�ѹ���Ķ������±���ʾ��
����
| ������������
| ��ѹ/V
|
Fe
| Fe? �� Cu
| +0.78
|
Zn
| Zn? �� Cu
| +1.10
|
A
| Cu? �� A
| ��0.15
|
B
| B? �� Cu
| +0.3
?
��������ʵ���¼�����������գ�
��1���������缫�Ľ���������Խ��ѹ���Ķ���Խ___________�������С������
Zn��A��B���ֽ��������ǿ������˳����__________________________��
��2��Cu��A��ɵ�ԭ��أ�_____Ϊ�������˵缫��ӦʽΪ___________________��
��3��A��B�γɺϽ�¶���ڳ�ʪ�����У�_______�ȱ���ʴ��
4��ѡ���� ���������ĸ�ͼ���˵������ȷ����
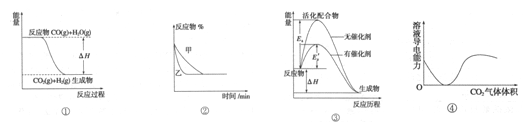
A��ͼ�ٱ�ʾ���淴ӦCO(g)+H20(g) 5C02 (g)+H2 (g)��H>0 5C02 (g)+H2 (g)��H>0
B��ͼ�ڱ�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g) 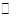 3C(g)+D(s)Ӱ�죬�ҵ�ѹǿ�� 3C(g)+D(s)Ӱ�죬�ҵ�ѹǿ��
C��ͼ�۱�ʾ��������ѧ��Ӧ�������仯
D��ͼ�ܱ�ʾC02ͨ�˱���̼������Һ�У���Һ�����Ա仯
5��ѡ���� ��A��B��C��D���ֽ�������A��B���ԭ���ʱ��������������A ��B ����A��D���ԭ���ʱ��AΪ������B��E����ԭ���ʱ���缫��ӦʽΪ��E2++2e-=E��B-2e-=B2+��A��??? B��D��E��������ǿ������˳��Ϊ��???��
A��D��A��B��E????????????????????? B��D��E��A��B
C��A��B��D��E????????????????????? D��A��B��E��D
|