微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
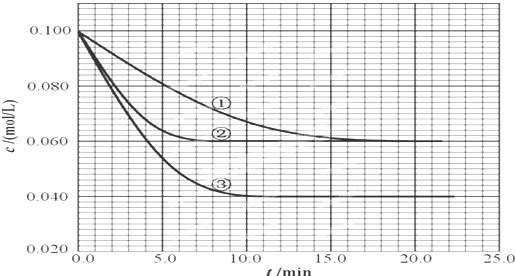
1、简答题 在2.00L的密闭容器中,反应2A(g)?B(g)+C(g)分别在三种不同实验条件下进行,但起始浓度相同,均为c(A)=0.100mol/L、c(B)=0.020mol/L及c(C)=0.020mol/L.反应物A的浓度随时间的变化如下图所示:
请回答下列问题:
(1)以下说法能说明该反应已达到平衡状态的是:______(填序号)
①c(A):c(B):c(C)=2:1:1
②v(A)=2v(B)
③体系的压强不再改变
④A的质量分数不再改变
⑤混合气体的密度不再改变
(2)根据实验③回答:反应开始到4.0min时反应物A的转化率为______,B平均反应速率为______.
(3)与①比较,②和③分别仅改变一种反应条件.所改变的条件是:②______;③______.
(4)实验①条件下该反应的化学平衡常数值是______.若实验①到达平衡后,维持体系温度不变,往容器中再投入0.028molB和0.028molC,求新平衡时体系中A的物质的量浓度.(写出计算过程)
参考答案:(1)①平衡时各物质的物质的量的多少取决于起始量与转化的程度
本题解析:
本题难度:一般
2、选择题 可逆反应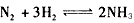 的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是 [???? ]
的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列各关系中能说明反应已达到平衡状态的是 [???? ]
A.3v正(N2) = v正(H2)
B.V正(N2)= v逆(NH3)
C.2v正(H2) = 3v逆(NH3)
D.v正(N2) = 3v逆(H2)
参考答案:C
本题解析:
本题难度:一般
3、选择题 在密闭容器中,反应X2(g)+2Y2(g)? ?2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
?2X Y2(g) ΔH<0达到甲平衡,若只改变某一条件再达到乙平衡,则对此过程条件改变的分析正确的是
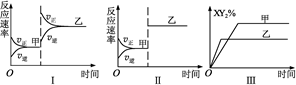
A.图Ⅰ由甲至乙加入适当催化剂
B.图Ⅱ由甲至乙扩大容器体积
C.图Ⅲ由甲至乙增大压强
D.图Ⅲ由甲至乙升高温度
参考答案:D
本题解析:
试题分析:A项:催化剂不能使化学平衡移动,故错;B项:化学平衡没移动,应该加入的是催化剂,故错;C项:增大压强,平衡正向移动,故错。故选D。
点评:本题考查温度温度、压强和催化剂对平衡移动的影响,题目难度中等,注意分析表中数据以及图象的曲线的变化,学习中注意加强该方面能力的培养。
本题难度:简单
4、简答题 原创工业上一般在恒容密闭容器中用H2和CO生产燃料甲醇,反应方程式为
CO(g)+2H2(g)

CH3OH(g)△H
(1)下表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250°C | 300°C | 350°C
K
2.041
0.270
0.012
①由表中数据判断△H______0(填“>”、“=”或“<“)
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为______,此时的温度为______.
(2)在100℃压强为0.1MPa条件下,容积为V?L某密闭容器中a?mol?CO与?2a?mol?H2在催化剂作用下反应生成甲醇,达平衡时CO的转化率为50%,则100℃该反应的平衡常数K=______(用含a、V的代数式表示并化简至最简单的形式).此时保持温度容积不变,再向容器中充入a?mol?CH3OH(g),平衡______(向正反应方向、向逆反应方向)移动,再次达到新平衡时,CO的体积分数______.(减小、增大、不变)
(3)要提高CO的转化率,可以采取的措施是______.
A.升温??????????????? B.加入催化剂????????????? C.增加CO的浓度
D.恒容充入H2 E.恒压充入惰性气体????????F.分离出甲醇
(4)判断反应达到平衡状态的依据是(填字母序号,下同)______.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(5)300°C,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡的有关数据如下:
| 容器 | 甲 | 乙 | 丙
| 反应物投入量
1molCO、2moL?H2
1molCH3OH
2molCH3OH
| 平
衡
时
的
数
据
CH3OH浓度(mol/L)
c1
c2
c3
反应的能量变化
akJ
bkJ
ckJ
体系压强(Pa)
p1
p2
p3
反应物转化率
α1
α2
α3
请选择正确的序号填空(不定项选择)
①c1、c2、c3的关系表达正确的为______
A??c3>2c1??????B?c1<c3<2c1??????C?c1=c2
②a、b、c的关系表达正确的为______
A???c<2|△H|B??a+b=|△H|C??c=2b
③p1、p2、p3的关系不正确的 为______
A??p1=p2??????B??p2<p3<2p2???????C??p3>2p2
④a1、a2、a3的关系表达不正确的为______
A??a1=a2???????B?a3<a2??????C??a1+a2=1.
参考答案:(1)①温度升高,K减小,说明升高温度平衡向逆反应方向移动,
本题解析:
本题难度:一般
5、选择题 可逆反应2SO2+O2?2SO3在恒温恒容下进行,能说明反应达到平衡的是( )
A.单位时间内消耗nmolSO2,同时生成nmolSO3
B.v逆(SO3)=2v正(O2)
C.容器内气体的密度保持不变
D.v(SO2)=v(SO3)
参考答案:A、单位时间内消耗n molSO2,同时生成n molSO3
本题解析:
本题难度:一般
|
|