微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 0.02mol・L―1的HCN溶液与0.02mol・L―1的NaCN溶液等体积混合,已知混合溶液中C(CN―)<C(Na+),则下列关系中,正确的是( )
A.C(Na+)>C(CN―)>C( H+)>C(OH
参考答案:
本题解析:
本题难度:一般
2、选择题 下列离子方程式属于盐的水解,且书写正确的是[???? ]
A.NaHCO3溶液:HCO3-+H2O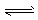 CO32-+H3O+
CO32-+H3O+
B.NaHS溶液:HS-+H2O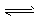 H2S+OH-
H2S+OH-
C.Na2CO3溶液:CO32- +2H2O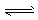 H2CO3+2OH-
H2CO3+2OH-
D.NH4Cl溶于D2O中:NH4++D2O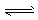 NH3・D2O+H+
NH3・D2O+H+
参考答案:B
本题解析:
本题难度:一般
3、填空题 已知:常温下,A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为 。
a.大于7 b.等于7 c.小于7
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为 mol/L,B溶液中水电离出的氢离子浓度为 mol/L。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为 。
参考答案:(1)b (2)10-10
本题解析:(1)pH=3的盐酸中的c(H+)与pH=11的氢氧化钡溶液中的c(OH-)相等,都等于1×10-3 mol・L-1,二者等体积混合后恰好完全反应,溶液呈中性。
(2)醋酸和氢氧化钠均抑制水的电离。
(3)a+b=14的意义为酸中c(H+)与碱中c (OH-)相等,二者混合后溶液呈碱性,说明碱为弱碱,反应中碱过量。故弱碱阳离子M+水解。
本题难度:一般
4、选择题 将0.1mol/L NaOH和0.1mol/L NH4Cl溶液等体积混合后,离子浓度大小正确的次序是:
A.C(Na+)>C(CI-)>C(OH-)>C(H+)
B.C(Na+)=C(CI-)>C(OH-)>C(H+)
C.C(Na+)=C(CI-)>C(H+)>C(OH-)
D.C(CI-)>C(Na+)>C(OH-)>C(H+)
参考答案:B
本题解析:由NaOH+NH4Cl=NaCl+NH3.H2O,得:反应后,变为等浓度的NaCl、NH3.H2O 溶液
NaCl=Na++Cl- (完全电离)??? NH3.H2O 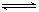 NH4++OH- (部分电离)
NH4++OH- (部分电离)
且溶液呈碱性,所以:C(OH-)>C(H+)
本题难度:简单
5、选择题 关于溶液中微粒的浓度,下列说法正确的是
A.0.1mol・L-1的(NH4)2SO4溶液中:c(SO42-) > c(NH4+) > c(H+) > c(OH-)
B.等浓度等体积的NaHSO3溶液与NaClO溶液混合后:c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + c(SO32-) + c(OH-)
C.等浓度等体积的NaHCO3溶液与NaCl溶液混合后:1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
D.标况下,将2.24L SO2气体通入到100ml 1mol・L-1的NaOH溶液中,完全反应后溶液呈酸性,则该溶液中:c(Na+) > c(HSO3-) > c(SO32-) >c(H+) > c(OH-)
参考答案:C
本题解析:
试题分析:A、(NH4)2SO4溶液中,NH4+水解程度较低,溶液呈酸性,离子的物质的量浓度关系为:c(NH4+) > c(SO42-)>c(H+)>c(OH-),错误;B、等浓度等体积的NaHSO3溶液与NaClO溶液混合后根据电荷守恒:c(Na+) + c(H+) = c(HSO3-) + c(ClO-) + 2c(SO32-) + c(OH-),错误。C、根据物料守恒可得1/2 c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3),正确;D、二者反应的化学方程式为:SO2+NaOH=NaHSO3,则该溶液中:c(Na+) > c(HSO3-) >c(H+) > c(SO32-) > c(OH-),错误。
考点:考查离子浓度大小比较。
本题难度:困难