微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 利用如图所示装置收集以下8种气体(图中烧瓶的位置不得变化)
①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
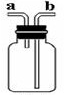
(1)若烧瓶是干燥的,则由b口进气收集的气体有???????????(写序号);
(2)若烧瓶充满水,可收集的气体有???????????????????????(写序号)。
(3)若在烧瓶内装入浓硫酸使气体干燥,则可用此装置来干燥的气体有________,这时气体由________口进入。
参考答案:(8分)(1)②④⑦⑧ (2)①③⑥?(3)①②③④⑥⑧??
本题解析:
试题分析:(1)若烧瓶是干燥的,则由b口进气收集的气体应该是密度大于空气的,所以符合条件的有氯气、氯化氢、H2S和SO2,NO极易被氧化生成NO2不能用排气法收集,答案选②④⑦⑧。
(2)若烧瓶充满水,可收集的气体应该是难溶于水的,则符合条件的是氢气、甲烷和NO,答案选①③⑥。
(3)若在烧瓶内装入浓硫酸使气体干燥,由于浓硫酸极易酸性和氧化性,则不能干燥碱性气体和还原性气态,则可用此装置来干燥的气体除了氨气和H2S外,其余均是可以的,即答案选①②③④⑥⑧,这时气体由b口进入,a口排出。
点评:常见气体的收集方法是:1.排水法,适用于不易溶于水的气体。例如氢气,氧气;2.向上排空气法,适用于比空气密度大,溶于水的气体,例如二氧化碳,氯气;3,向下排空气法,适用于比空气密度小,溶于水的气体,例如氨气。
本题难度:一般
2、实验题 (15分)已知NaHCO3低温时溶解度小。德榜制碱的方法是:向氨化的饱和食盐水中通入过量的二氧化碳,即有晶体析出,经过滤、洗涤、焙烧得纯碱。此过程可以表示为:
①NaCl(饱和)+NH3+CO2+H2O=NaHCO3↓+NH4Cl(此反应是放热反应)
②2NaHCO3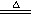 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
现某化学小组根据上述原理在实验室中模拟制碱过程,下图C装置是溶有氨和NaCl的溶液,且二者均达到了饱和。
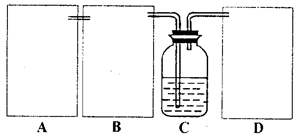
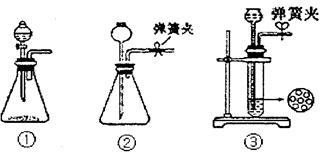
(1)制CO2时为了使反应随开随用,随关随停,上图A方框内应选用以下_________装置(填序号)。简述该装置能随关随停的理由________________。
(2)为使实验能够进行,在B、D方框内补上所需装置:_________________(将装置图画在答题卡上),并指明所用试剂:_________________。
(3)该小组同学按正确的方法连接装置,检验气密性合格后进行实验,发现析出的晶体非常少。老师的指导下,他们对某个装置进行了改进,达到了实验目的。你认为他们的改进方法是___________________。
(4)若所用饱和食盐水中含有NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.46g,假设第二步分解时没有损失,则Na2CO3的产率为______________。
参考答案:(1)③(1分),关闭弹簧夹后反应生成的气体使上部压强增大,
本题解析:(1)实验室制取二氧化碳一般采用块状大理石和盐酸反应,要使反应随开随用,随关随停,关键是使固体和溶液分离才能到达目的,故一般采用简易启普发生器,即装置③。原因是关闭弹簧夹后反应生成的气体使上部压强增大,到达一定程度后可把反应液压回漏斗,使固液分离从而停止反应。
(2)因为生成的二氧化碳气体混有氯化氢气体,再通入到C之前要先除杂,试剂选用饱和的碳酸氢钠溶液。由于氨气极易溶于水,所以为了防止倒吸,需要加入1个防倒吸的装置,试剂可以是水或者稀硫酸。
(3)因为NaHCO3低温时溶解度小,所以要大量析出,需要降低溶液的温度。
(4)NaCl的质量为5.85g,所以根据原子守恒可知理论上应得到8.4g碳酸氢钠。由于第二步分解时没有损失,所以Na2CO3的产率是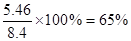 。
。
本题难度:一般
3、实验题 (14分)氯化铜晶体(CuCl2・xH2O)是重要的化工原料,可用作催化剂、消毒剂等。用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:

⑴酸溶时,为了提高浸取率可采取的措施有????????????????。(写出一点)
⑵若溶液A含有的金属离子有Cu2+、Fe2+,则试剂①为Cl2,通入Cl2发生反应的离子方程式:?????????????????????????????。
⑶加入试剂②的目的是调节pH至a,a的范围是??????????;
为避免引入杂质离子,试剂②可选用??????????????。
A.氨水
B.氧化铜
C.氢氧化铜
D.氢氧化钠
⑷由溶液C获得CuCl2・xH2O,实验操作依次是加热浓缩、冷却结晶、过滤和洗涤等操作。加热浓缩过程需加入少量盐酸的目的是:??????????????????????????????????。
⑸工业生产过程会产生含Cu2+的废水,向废水加入碱调节pH=8,沉降后废水中Cu2+浓度为????????????????mol/L。(已知Ksp[Cu(OH)2]=5.6×10-20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl2溶液中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制备CuCl的离子方程式:??????????????????????????????。
参考答案:(14分)
⑴粉碎孔雀石或适当升高温度或搅拌或适当提高
本题解析:
试题分析:⑴酸溶时,为了提高浸取率可采取的措施有粉碎孔雀石或适当升高温度或搅拌或适当提高酸的浓度。
⑵若溶液A含有的金属离子有Cu2+、Fe2+,则试剂①为Cl2,使亚铁转化为三价铁,通入Cl2发生反应的离子方程式:2Fe2++Cl2 = 2Fe3++ 2Cl-。
⑶加入试剂②的目的是调节pH至a,a的范围是3.7~5.4保证铁离子沉淀完全;
为避免引入杂质离子,试剂②可选用:氧化铜?;氢氧化铜 。
⑷由溶液C获得CuCl2・xH2O,实验操作依次是加热浓缩、冷却结晶、过滤和洗涤等操作。加热浓缩过程需加入少量盐酸的目的是:抑制CuCl2 水解。
⑸工业生产过程会产生含Cu2+的废水,向废水加入碱调节pH=8,C(OH-)=1×10-6所以沉降后废水中Cu2+浓度=Ksp[Cu(OH)2]/C2(OH-)=5.6×10-8mol/L。(已知Ksp[Cu(OH)2]=5.6×10-20)
⑹氯化亚铜(CuCl)也是一种重要的化工原料。
制备过程:向CuCl2溶液中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。制备CuCl的离子方程式:2Cu2++2Cl-+SO2+2H2O 2CuCl↓+4H++SO42-。
2CuCl↓+4H++SO42-。
点评:此题综合性较强,能够考查学生把所学知识运用到实际问题的能力。
本题难度:一般
4、选择题 配制100mL0.5mol/LNaOH溶液的操作有?①计算 ②冷却 ③洗涤 ④溶解 ⑤转移 ⑥称量?⑦定容,次序正确的是
A.①⑥③②⑤④⑦
B.①⑥④⑤②③⑦
C.①⑥④②⑤③⑦
D.①⑥③④⑤②⑦
参考答案:C
本题解析:
试题分析:配置溶液的一般步骤是计算、称量、溶解、冷却、转移、洗涤、定容。
点评:此题考核了溶液配置的步骤,熟悉实验操作步骤,难度不大。
本题难度:简单
5、实验题 (8分)用如下图所示(夹持仪器省略)的装置进行实验,将液体A逐滴加入到固体B中,回答下列问题:
①下图中D装置在实验中的作用是__________________________________________;
②若A为浓盐酸,B为KMnO4,C为淀粉KI溶液,旋开E后,C中的现象为____________________,反应的化学方程式是______________________________________;
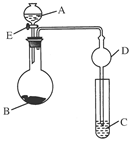
③若A为浓硫酸(70%),B为Na2SO3,C为酸性KMnO4溶液,旋开E后,C中的现象为________________________________________________________________________,
反应的化学方程式是_______________________________________________;
④若A为30%H2O2溶液,B为MnO2;C为H2S饱和溶液,旋开E后,C中的现象为________________________________________________________________________,
反应的化学方程式是__________________________________________________;
⑤若A为稀盐酸,B为大理石,C为Na2SiO3溶液,旋开E后,C中的现象为________________,反应的化学方程式是__________________________________;
⑥上图所示装置有多种用途,请举例(除题中之外):A为________,B为________,C中盛________,旋开E后,C中的现象为________________,反应的化学方程式是________________________________________________________________________。
参考答案:①防止溶液倒吸"②溶液先变蓝后褪色"2KI+Cl2===2K
本题解析:同一装置,多种用途,考查学生灵活运用知识的能力、开拓学生视野。
本题难度:一般