微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 你认为下列数据可信的是[???? ]
A.某溶液中溶质的质量分数超过100%
B.某常见气体的密度为1.8g/cm3
C.某澄清石灰水的浓度是2.0mol/L
D.某元素的原子半径是0.160nm
2、简答题 (化学-选修化学与生活模块)
碘缺乏症遍及全球,多发生于山区,南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区.我国云南、河南等l0余省的山区发病率也较高.为控制该病的发生,较为有效的方法是食用含碘食盐.我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3).据此回答下列问题.
(1)碘是合成下列哪种激素的主要原料之一______
A.胰岛素????B.甲状腺激素??????C.生长激素????D.雄性激素
(2)可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾.反应的化学方程式为______,氧化产物与还原产物的物质的量之比为______,能观察到的明显现象是______.
(3)已知KIO3可用电解法制得.原理:以石墨为阳极,以不锈钢为阴极,在一定电流强度和温度下电解KI溶液.总反应方程式为Kl+H2O
?电解?
.
?
KlO3+3H2↑,则阴极反应式为:______.
(4)在某温度下,若以l2A的电流强度电解KI溶液l0min,理论上可得标准状况下氢气______L(一个电子的电量为1.60×10-19C).
3、填空题 某课外实验小组设计了如图所示装置进行“一器多用”的实验探究(夹持装置已略去).
(1)该小组同学用该装置进行“H2的制取及燃烧性质验证”实验.他们设计了如下的实验步骤:
a.组装装置并检验气密性
b.装入药品,关闭活塞m和n,固定在铁架台上
c.打开分液漏斗活塞m,使反应开始
d.当观察到B中有较多气体时,打开活塞n并点燃气体
回答下列问题:
①以上某步骤中有一处明显的操作错误,请指出错误之处______
②该小组同学在进行c步骤操作时,发现分液漏斗中的溶液不能滴下,你认为可能的原因有______.
(2)该装置还可用于制取并收集少量其他气体,用字母代号填空:下列气体中哪些可以用该装置来制取和收集______;若将装置B中的水换成CCl4,下列气体中哪些可以用该装置来制取和收集______.
A.O2 B.NO C.SO2 D.NH3 E.C2H2 F.C2H4
(3)该小组同学用该装置进行定量实验,以确定某稳定饱和脂肪醇的结构.
①反应前,先对量气管进行第一次读数,读数为40.0mL,然后在A中加入5gNa和0.62g待测醇,充分反应后,再进行第二次读数,读数为264.0mL(所有数据均已换算成标准状况时的数值).读数时要注意的是:一是使视线与凹液面最低处相平,二是______.
②为了进一步确定该醇的结构,又将0.62g该醇充分燃烧,可以生成0.02mol的CO2和0.03mol的H2O,已知两个或者两个以上的羟基连在同一个C原子上不能形成稳定的醇,根据上述信息计算确定该饱和醇的结构简式为______.
4、填空题 食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下
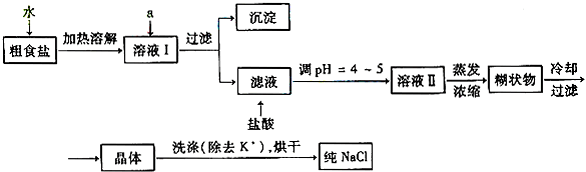
提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
① 欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为__________
(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为___________ _______。
(2)用提纯的NaCl配制500mL4.00 mol・L-1NaCl溶液
① 本次实验所用仪器除药匙、玻璃棒外还有_____________(填仪器称)。
②用托盘天平称取的NaCl晶体的质量为:_____________;
③在配制溶液的过程中多次用到玻璃棒,在溶解时玻璃棒的作用是:_____________, 在移液时玻璃棒的作用是:__________________。
④观察液面时,若俯视刻度线,会使所配制的溶液的浓度_________(填“偏高”、“偏低” 或“无影响”,下同);加蒸馏水时不慎超过了刻度线后倒出部分溶液,使液面与刻度线相切,会__________;
(3)用ρ=1.84g・mL-1,质量分数为98%的浓硫酸配制200mL1mol・L-1的稀硫酸与上述配制溶液的步骤上的差别主要有三点:
①计算:理论上应取浓硫酸的体积V=___________mL(精确到小数点后两位);
②量取:由于量筒是一种粗略的量具,如想精确量取,必需选用_____________(填仪器名称)。
③溶解:稀释浓硫酸的方法_________________________________________。
5、选择题 下列实验方案中,不能测定Na2CO3和NaHCO3,混合物中Na2CO3质量分数的是(?? ) A.取a?g混合物充分加热,剩余b?g固体
B.取a?g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b?g固体
C.取a?g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b?g
D.取a?g混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b?g固体
|
网站客服QQ: 960335752 - 14613519 - 791315772