微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,下列装置是用燃烧法确定有机物分子式常用的装置。?

(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是____。
(2)C装置中浓硫酸的作用是____。
(3)D装置中MnO2的作用是____。
(4)燃烧管中CuO的作用是____。
(5)若准确称取0.90 g样品(含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32 g,B管质量增加 0.54 g,则该有机物的实验式为____。
(6)要确定该有机物的分子式,还要知道__________。
参考答案:(1)g-f,e-h,i-c(或d),d(或c)-a(或b)
本题解析:
本题难度:一般
2、选择题 下列叙述正确的是
 [???? ]
[???? ]
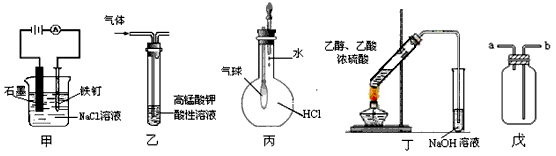
①装置甲可防止铁钉生锈 ②装置乙可除去乙烯中混有的乙炔 ③装置丙可验证HCl气体在水中的溶解性 ④装置丁可用于实验室制取乙酸乙酯 ⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体
A.①③⑤
B.③⑤
C.①②④
D.③④
参考答案:B
本题解析:
本题难度:一般
3、选择题 为了除去粗盐中的Ca2+?和SO42-,可将粗盐溶于水,然后进行下列操作:
①过滤;
②加适量的盐酸;
③加过量的Na2CO3溶液;
④加过量BaCl2溶液.
正确的操作顺序是( )
A.①③④②
B.③①④②
C.①②③④
D.④③①②
参考答案:D
本题解析:
本题难度:一般
4、实验题 碱式碳酸铜可表示为:xCuCO3・y Cu(OH)2・zH2O,测定碱式碳酸铜组成的方法有多种。现采用氢气还原法,请回答如下问题:
(1)写出xCuCO3・yCu(OH)2・zH2O与氢气反应的化学方程式_______________________;
(2)实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)一( )( )一( )( )一( )( )一( )( )一( )( )一(l)

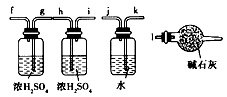
(3)称取23. 9g某碱式碳酸铜样品,充分反应后得到12. 7g残留物,生成4.4g二氧化碳和7.2g水。该样品的结晶水质量为__________g,化学式为_________________;
(4)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由。 _________________________________________________
参考答案:(1)xCuCO3・yCu(OH)2・zH2O+(x+y)H
本题解析:
本题难度:困难
5、填空题 图中,甲由C、H、O三种元素组成,元素的质量比为12:3:8,甲的沸点为78.5℃,其蒸气与H2的相对密度是23.将温度控制在400℃以下,按要求完成实验.
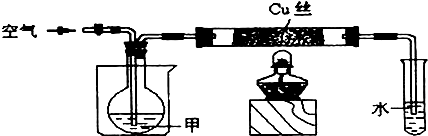
(1)在通入空气的条件下进行实验Ⅰ.
①甲的名称是______,加入药品后的操作依次是______.
a.打开活塞
b.用鼓气气球不断鼓入空气
c.点燃酒精灯给铜丝加热
②实验结束,取试管中的溶液与新制的Cu(OH)2混合,加热至沸腾,实验现象为______写出发生反应的化学方程式______
(2)在停止通入空气的条件下进行实验Ⅱ.
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是______.
②甲蒸气进入反应管后,在铜做催化剂有250-350℃条件下发生可逆的化学反应,在试管中收集到了实验Ⅰ相同的产物,并有可燃性气体单质放出.该反应揭示了甲催化氧化的本质.写出实验Ⅱ中反应的化学方程式______,并结合该化学方程式简要说明实验Ⅰ中所通空气的作用______
(3)甲也是一种良好的有机溶剂.某同学在进行溴乙烷与NaOH的甲溶液的反应中,观察到有气体生成.请设计一种实验方案检验该气体,完成下列表格.
| 操作方法及所用试剂 | 实验现象
______
______
参考答案:(1)①甲由C、H、O三种元素组成,元素的质量比为12:3:
本题解析:
本题难度:一般
|