微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)按要求填空:
(1)0.2molO3和0.3molO2的质量 (选填“相等”、“不相等”或“无法判断”),分子数之比为 ,所含原子数之比为 ,在相同条件下的体积之比为 。
(2)73g HCl气体中含有 个分子,标准状况下占有的体积为 L。
(3)相同物质的量浓度的KCl、CuCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3
2、选择题 配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因可能是( )
A.容量瓶中原来含有少量蒸馏水
B.烧杯中溶解NaOH后,未经冷却,立即转移至容量瓶并洗涤烧杯,定容
C.溶解NaOH的烧杯没有洗涤
D.向容量瓶中加水定容时眼睛一直仰视刻度线
3、实验题 下图是硫酸试剂瓶标签上的内容。
硫酸:化学纯(CP)(500mL)
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84g・cm-3
质量分数:98%
(1)该硫酸的物质的量浓度为???????????;
(2)实验室用该硫酸配制240mL 0.46mol/L的稀硫酸,则
①有以下仪器: A.烧杯 B.100mL量筒 C.250mL容量瓶 D.500mL容量瓶 E.玻璃棒 F.托盘天平(带砝码)G.10mL量筒H.胶头滴管,配制时,必须使用的仪器有??????????(填代号).
②需要该硫酸的体积为?????????mL.
③下图为配制过程中的几个关键步骤和操作:将上述实验步骤A―F按实验过程
先后次序排列????????????????。
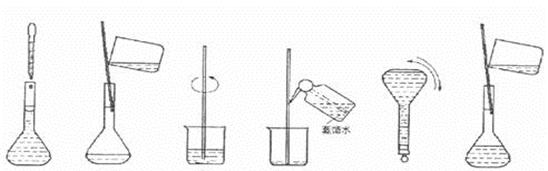 蒸馏水
?
A????????? B??????????? C?????????? D??????????????? E????????? F
④该同学实际配制得到的浓度为0.45mol/L,可能的原因是???????
A.量取浓H2SO4时仰视刻度
B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶
D.定容时仰视刻度
4、填空题 (5分)下图为某市售盐酸试剂瓶标签上的部分数据。问:

(1)该盐酸的物质的量浓度为多少?
(2)取该盐酸25.4 mL与2.00 mol・L-1的氢氧化钠
溶液100 mL混合,再将混合液稀释到1.00 L,
此时溶液的pH约为多少?
5、选择题 设NA是阿伏加德罗常数的值,下列说法正确的是
A.1 L1mol・L-1的NaClO溶液中含有ClO-的数目为NA
B.60g二氧化硅含有的共价键数为2NA
C.7.8g钾与100mL 1mol・L-1盐酸充分反应生成气体分子数为0.1NA
D.标准状况下,7.1g 氯气与足量的石灰乳充分反应,转移电子数为0.2NA
|
|
网站客服QQ: 960335752 - 14613519 - 791315772