微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,下列溶液中一定能大量共存的离子组是( )
A.含有大量S2-的溶液:ClO-、Na+、Cl-、CO32-
B.无色澄清溶液:MnO4-、SO42-、K+、Fe3+
C.能使pH试纸变红的溶液:NH4+、Na+、SO42-、Fe3+
D.水电离产生的c(H+)=1×10-12mol/L的溶液:HCO3-、NH4+、Cl-、Ca2+
参考答案:A、因S2-与ClO-发生氧化还原反应而不能大量共存,故A错
本题解析:
本题难度:一般
2、选择题 下列各组离子,在强碱性溶液中可以大量共存的是?? [???? ]
A.Na+、Ba2+、Cl-、SO42-???????????
B.Na+、Ba2+、AlO2-、NO3- ???
C.NH4+、K+、Cl-、NO3-?????????????
D.Na+、K+、NO3-、SiO32-
参考答案:BD
本题解析:
本题难度:一般
3、选择题 已知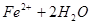

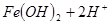 ,则往浅绿色的
,则往浅绿色的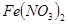 溶液中逐滴加入稀盐酸,溶液颜色的变化情况是
溶液中逐滴加入稀盐酸,溶液颜色的变化情况是
A.变为深绿色
B.变为黄棕色
C.褪为无色
D.没有颜色变化
参考答案:B
本题解析:因为在酸性条件下,NO3-能氧化Fe2+,生成Fe3+,所以溶液颜色会变成棕黄色,答案选B。
本题难度:简单
4、选择题 在给定的四种溶液中,含有以下各种微粒,一定能大量共存的是? (?? )
A.由水电离的c(OH-)=1×10-12mol/L的溶液中:Ba2+、K+、Br-、SiO32-
B.常温下葡萄糖溶液中:SCN―、Cl-、K+、NH4+
C.溴水中:Na+、CO32-、NH4+、SO42―
D.PH大于7的溶液: Na+、Ba2+、SO32-、ClO―
参考答案:B
本题解析:
试题分析:A、在室温下纯水电离产生的c(OH-)=1×10-7mol/L.现在由水电离的c(OH-)=1×10-12mol/L说明溶液中存在大量的H+或OH-,对水的电离起到了抑制作用。若溶液显酸性,则发生反应2H++SiO32-=H2SiO3↓。离子不能电离共存。错误。B、常温下葡萄糖溶液中:SCN―、Cl-、K+、NH4+与葡萄糖分子不会发生任何反应,,可以大量共存。正确。C、溴水显酸性,这时会发生反应:2H++CO32-=H2O+CO2↑。不能大量共存。错误。D.发生沉淀反应Ba2++SO3
本题难度:一般
5、选择题 下列说法错误的是
A.将pH=4的醋酸稀释后,溶液中所有离子的浓度均减小
B.pH=11的某溶液中,水的电离可能促进也可能是抑制
C.改变条件使醋酸的电离平衡向右移动,醋酸的电离度可能增大也可能减小
D.改变条件使醋酸钠溶液中的醋酸根离子浓度增大,溶液的pH可能减小也可能增大
参考答案:A
本题解析:考查弱电解质的电离平衡:CH3COOH CH3COO-+H+,它受浓度、温度、酸、碱及盐等外界条件的影响,可发生移动
CH3COO-+H+,它受浓度、温度、酸、碱及盐等外界条件的影响,可发生移动
A:酸溶液稀释后,酸性减弱,c(H+)减小,而c(OH―)一定增大,排除
B:正确
C:例如升温促进其电离,而增大其浓度刚抑制其电离,正确
D:例如向溶液中加入醋酸钠固体,
本题难度:简单