��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڳ�����0.1mol��L��1 NaHCO3��Һ��������������ȷ���ǣ�???��
A��c (Na��)="c" (HCO3��) + c (CO32��) + c (H2CO3)
B���¶����ߣ���Һ��pH���ߣ�����Һ�е�c��H������c��OH�����˻�����
C����������Ũ�ȵ�CH3COOH��Һ��Ӧ����Һ��c��Na������c��CH3COO����
D������������NaOH���壬��Һ��pH��С
�ο��𰸣�BD
���������
���������A����������غ�ԭ������ʾ��Ԫ�ص���Ũ��ʼ����̼Ԫ�ص���Ũ����ȣ���A��ȷ��B�̼��������ǿ�������Σ���ȫ�������̼��������ӵ�ˮ��̶ȴ��ڵ���̶ȣ����Ը�����Һ�������ԣ�����̼��������ӵ�ˮ�ⷴӦ�����ȷ�Ӧ�������¶ȣ��ٽ���ˮ��ƽ�����ƣ�����������Ũ��������Һ�ļ�����ǿ��pH���ߣ�ͬʱ���ܼ�ˮ�ĵ���Ҳ�����ȷ�Ӧ�������¶ȣ��ٽ�ˮ�ĵ��룬��ˮ�����ӻ�������Һ�е�c��H������c��OH�����˻����¶����߶�����B����������NaHCO3+CH3COOH=CH3COONa+CO2��+
�����Ѷȣ�һ��
2��ѡ���� ������ɫ����Һ���ܴ���������ǣ�
[???? ]
A��K+��Na+��Cl-��HCO3-��OH-
B��Cl-��NO3-��MnO4-��K+��Na+
C��SO42-��K+��Mg2+��Cl-��NO3-
D��H+��Cl-��Br-��HS-��K+
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ��һ����������Һ��ֻ���ܺ���Fe3+��Fe2+��H+��AlO2-��Al3+��CO32-��NO3-���������еļ��֣�����Һ����μ���һ����1mol/L��NaOH��Һ�Ĺ����У���ʼû�г����������г����������ж���ȷ����
A��һ�㲻��Fe3+��Fe2+
B����Һ���ܺ���AlO2-
C����Һ���ܺ���NO3-
D�����ܺ���Fe3+ ��һ������Fe2+
�ο��𰸣�D
�����������
�����Ѷȣ���
4������� ������������A��B��C��D��E�����ǵ������ӿ�����Na����NH4+��Cu2����Ba2����Al3����Ag����Fe3���������ӿ�����Cl����NO3-��SO42-��CO32-����֪��
�������ξ�����ˮ��ˮ��Һ��Ϊ��ɫ��
��D����ɫ��Ӧ�ʻ�ɫ��
��A����Һ�����ԣ�B��C��E����Һ�����ԣ�D����Һ�ʼ��ԡ�
�������������ε���Һ�зֱ����Ba(NO3)2��Һ��ֻ��A��C����Һ������������
�������������ε���Һ�У��ֱ���백ˮ��E��C����Һ�����ɳ����������Ӱ�ˮ��C�г�����ʧ��
�ް�A����Һ�ֱ���뵽B��C��E����Һ�У��������ɲ�����ϡ����ij�����
��ش��������⣺
��1���������У�һ��û�е���������____________��������������ͬ�������εĻ�ѧʽ��__________________��
��2��D�Ļ�ѧʽΪ__________________��D��Һ�Լ��Ե�ԭ����_________________(�����ӷ���ʽ��ʾ)��
��3��A��C����Һ��Ӧ�����ӷ���ʽ��______________________________________��
E�Ͱ�ˮ��Ӧ�����ӷ���ʽ��____________________________________________��
��4����Ҫ����B�������������ӣ���ȷ��ʵ�鷽����______________________________��
�ο��𰸣���1��Cu2����Fe3����(NH4)2SO4��Al2(SO4
�����������������Һû����ɫ������û��Cu2����Fe3��������ʵ�������֪��A��B��C��D��E�ֱ�ΪBaCl2��(NH4)2SO4��AgNO3��Na2CO3��Al2(SO4)3������NH4+�����õķ����ǽ������ŨNaOH��Һ���ȣ����Ƿ��ܹ�����ʹʪ��ĺ�ɫʯ����ֽ���������塣
�����Ѷȣ�һ��
5��ѡ���� �����£����и���������ָ����Һ��һ���ܴ���������ǣ�????��
A����ɫ��Һ�У�K+��Na+��Cu2+��SO42��
B��c(H��)/c(OH��)��1��10��14����Һ��K����Na����Cl����SiO32��
C����ˮ�������C(OH��)=1��10-12 mol��L��1����Һ��NH4+��HCO3����Na+��Cl��
D��c(OH��)��10��13 mol��L��1����Һ�У�Al3+��NO3����I����Cl��
�ο��𰸣�B
���������
���������A��Cu2+����ɫ��������ɫ��Һ���������£�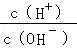 =1��10��14����Һ��c��OH����=1mol/L����Һ�Լ��ԣ���������֮�䲻��Ӧ����Bѡ����������ˮ�������c��H+��=10��12mol?L��1����Һ��Ϊ������Һ������Һ����HCO3���ȷ�Ӧ��������Һ��HCO3����NH4+���ܹ��棬��C��ѡ��
=1��10��14����Һ��c��OH����=1mol/L����Һ�Լ��ԣ���������֮�䲻��Ӧ����Bѡ����������ˮ�������c��H+��=10��12mol?L��1����Һ��Ϊ������Һ������Һ����HCO3���ȷ�Ӧ��������Һ��HCO3����NH4+���ܹ��棬��C��ѡ��
�����Ѷȣ�һ��