��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���������ӵĵ�����ڹ�ҵ�Ͽ��õ��KI��Һ��ȡ���缫������ʯī�Ͳ���֣���ѧ����ʽ�ǣ�KI��3H2O KIO3��3H2�����й�˵������ȷ����
KIO3��3H2�����й�˵������ȷ����
A��ʯī�������������������
B��I-�������ŵ磬H+�������ŵ�
C���������е������Һ��pH��С
D�����ת��3 mol e-ʱ�������Ͽ��Ƶ�KIO3 107 g
�ο��𰸣�C
���������
���������A�����ݷ���ʽ��֪������ʧȥ���ӣ�ˮ������������ӵõ�����ת��Ϊ����������������ʧȥ���ӣ������õ����ӣ����Ըõ����������Ƕ��Ե缫����ʯī���������������������A��ȷ��B������A�з�����֪I-�������ŵ磬H+�������ŵ磬B��ȷ��C�����ʱ�����ӷŵ磬�Ӷ������������������Һ�ļ�����ǿ����pH���C����D�����ݷ���ʽ��֪����1mol�����ת��6mol���ӣ�����ת��3 mol e-ʱ�������Ͽ��Ƶ�KIO3��������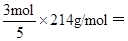 107g��D��ȷ����ѡC��
107g��D��ȷ����ѡC��
���㣺������ԭ����Ӧ��
�����Ѷȣ�һ��
2��ѡ���� ��ˮ�м�������ʵ�����Ag����Pb2����K����SO42����NO3����Cl�����ö��Ե缫������Һ�����ռ����������������������뻹ԭ���������֮��Ϊ��???����
A��35.5:108
B��16:207
C��108:35.5
D�� 8:1
�ο��𰸣�D
���������
����������������ӷ�Ӧ������������֪����ˮ�м�������ʵ�����Ag����Pb2����K����SO42����NO3����Cl���������Ȼ���������Ǧ��ɫ����������Һʵ��ʱ�������Һ�����Ե���ʵ��ʱ�ǵ��ˮ��������������������ԭ���������������ߵ�����֮��Ϊ16�U2����ѡD��
����������Ĺؼ������ȸ������ӹ��棬�ó���Һ�д��ڵ��������ӣ�Ȼ�����жϼ��ɡ��������׳��ֵ������ǣ�ֱ���������ӵķŵ�˳���ж���������ͻ�ԭ����Ӷ��ó�����Ľ��ۡ������������֪ʶ������Ҫ�ġ�
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ����
A�����ϡ������Һ����Һ��Ũ�Ȼ����pH���
B���ȼҵ�У���·��ÿת��1mol���ӣ��������ռ���1mol����
C�������Ȼ�����Һ���õ�ϡ��Һ�У�����Ũ���ᣬ�ָܻ���ԭ��ҺŨ��
D����ͭ����ʱ����ͭӦ�����ص��������������Һ�ڵ�������Ũ�Ȳ���
�ο��𰸣�B
���������
���������A�����Ե缫���ϡ������Һ���൱���ǵ��ˮ����Һ��Ũ�Ȼ������������ǿ������pH��С��A����ȷ��B���ȼҵ�У���·��ÿת��1mol���ӣ������������������ֱ��ռ���0.5mol������0.5mol���������ռ���1mol���壬B��ȷ��C�����Ե缫��ⱥ��ʳ��ˮ���õ��������ơ����������������������Ȼ�����Һ���õ�ϡ��Һ�У�ͨ���Ȼ������壬�ָܻ���ԭ��ҺŨ�ȣ�C����ȷ��D��D����ͭ����ʱ����ͭӦ�����ص������������ڴ�ͭ�к���п�����Ȼ�����ǿ��ͭ�����ʣ�����п����������ʧȥ���ӣ���
�����Ѷȣ�һ��
4�������� �ö��Ե缫���NaCl��CuSO4�Ļ����Һ250 mL������һ��ʱ�������������11.2 L(��״�������壬��ԭ��Һ��Cu2+��Cl-�����ʵ���Ũ�ȷ�Χ��
�ο��𰸣�0<c(Cu2+)<2 mol��L
����������������⣬�������ŵ��������Cu2+��H+���������ŵ��������Cl-��OH-����ֻ��Cl-�ŵ磬�������������ɵ����岻����һ���ࣩ����c(Cl-)=x,c(Cu2+)=y��
������Ӧ
Cu2+?????? +?????? 2e- C
C
�����Ѷȣ���
5��ѡ���� pH��a��ij�������Һ�У�������ֻ���Ե缫��ֱͨ����һ��ʱ�����Һ��pH��a����õ���ʿ����� (����)
A��H2SO4
B��AgNO3
C��Na2SO4
D��NaOH
�ο��𰸣�D
���������
���������A�����ڵ��H2SO4��˵��ʵ�ʾ��ǵ��ˮ������ֱͨ����һ��ʱ�����Һ��pH��С������B�����ڵ��AgNO3��˵�������ܷ���ʽ��4AgNO3+2H2O 4Ag+O2��+4HNO3�����ֱͨ����һ��ʱ�����Һ��pH��С������C. Na2SO4��ǿ��ǿ���Ρ�ʵ���ǵ��ˮ��ֱͨ����һ��ʱ���
4Ag+O2��+4HNO3�����ֱͨ����һ��ʱ�����Һ��pH��С������C. Na2SO4��ǿ��ǿ���Ρ�ʵ���ǵ��ˮ��ֱͨ����һ��ʱ���
�����Ѷȣ�һ��