微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将22.4g金属粉末混合物,放入足量的稀H2SO4中至无气泡产生为止,共收集到标准状况下的H2 22.4L,此混合物可能是(??)
A.锌和铜
B.镁和铁
C.铝和锂
D.锌和铝
参考答案:D
本题解析:当收集到标准状况下的H2 22.4L时,转移了2mol电子,此时金属的平均摩尔质量为22.4g/mol,肯定金属混合物中,有一种金属比22.4大,一种比22.4小。
A 错误,锌和铜的摩尔质量分别为65 g/mol、64 g/mol,都比22.4g/mol大,不可能
B 错误,镁和铁的摩尔质量分别为24 g/mol、56 g/mol,都比22.4g/mol大,不可能
C 错误,铝和锂的摩尔质量分别为18 g/mol、7 g/mol,都比22.4g/mo小,不可能
D 正确,锌和铝的
本题难度:一般
2、选择题 下列物质不能通过化合反应直接制得的是(??)
A.FeCl2
B.NaHCO3
C.Al(OH)3
D.Fe(OH)3
参考答案:C
本题解析:A项,Fe+2FeCl3=3FeCl2;B项,Na2CO3+CO2+H2O=2NaHCO3;C项,通过化合反应不能直接制得Al(OH)3;D项,4Fe(OH)2+O2+2H2O=4Fe(OH)3,故选C项。
本题难度:一般
3、填空题 (16分)提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
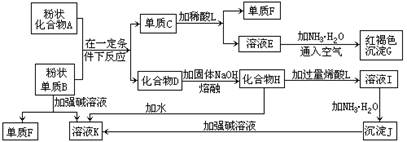
(1)单质F的化学式为?????????????。 (2)溶液I中所含金属离子是?????????????。
(3)由E生成G的反应类型为????????????????????,????????????????????;?
A和B的混合物称为?????????????????????????。
(4)写出下列离子方程式: C+L?????????????????????????????????????????;
H转变成I??????????????????????????????????????????????;
I转变成J??????????????????????????????????????????????;
(5)由C→E+F若改用浓酸,则不能选用的浓酸是(写分子式)???????????????。
参考答案:(1)H2????(2)Al3+和Na+???(3) 复分解
本题解析:
试题分析:(1)中学阶段所学的能和烧碱反应产生氢气的金属单质只有铝,故单质B为铝,单质F为氢气,溶液K为四羟基合铝酸钠,红褐色沉淀G为氢氧化铁,故溶液E为含有亚铁离子的盐,故C为铁,A为铁的氧化物,D为氧化铝,化合物H为四羟基合铝酸钠固体,L为含有铝离子的盐,沉淀J为氢氧化铝;
(2)溶液I为四羟基合铝酸钠溶液,它与过量稀酸反应生成的钠盐和铝盐,故填:Na+、Al3+;
(3)亚铁盐和碱反应生成氢氧化亚铁,然后被空气迅速氧化,Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+、4
本题难度:困难
4、填空题 金属铁分别与单质Cl2和Br2反应可得无水FeCl3和FeBr3,当把铁粉与碘粉混合一起研磨时,生成相当于Fe3I8的产物,则在此产物中铁的化合价是________;若将Fe3I8改写成常见碘化物的形式,其化学式为是_________________。
参考答案:+2、+3FeI2・2FeI3
本题解析:在Fe3I8中,n(Fe)∶n(I)=3∶8,因为1∶3<3∶8<1∶2,所以,铁的化合价为+2、+3。
本题难度:简单
5、选择题 一定体积的18 mol/L的硫酸中加入过量铜片,加热,被还原的硫酸为0.9 mol,则浓硫酸的实际体积为
A.等于50 mL
B.大于50 mL
C.等于100 mL
D.大于100 mL
参考答案:D
本题解析:
试题分析:由于铜和浓硫酸的反应过程中,随着反应的进行,硫酸的浓度逐渐降低,而稀硫酸与铜不反应,所以根据反应式Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑可知,如果被还原的硫酸为0.9 mol,则实际参加反应的硫酸的物质的量大于1.8mol,因此浓硫酸的实际体积大于100ml,答案选D。
CuSO4+2H2O+SO2↑可知,如果被还原的硫酸为0.9 mol,则实际参加反应的硫酸的物质的量大于1.8mol,因此浓硫酸的实际体积大于100ml,答案选D。
本题难度:简单