微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关金属的说法正确的是(??)
A.金属原子只有还原性,金属阳离子只有氧化性
B.金属单质在常温下都是固体
C.含金属元素的离子都是阳离子
D.金属阳离子被还原不一定得到金属单质
参考答案:D
本题解析:
试题分析:金属原子只有还原性,因为在反应过程中,金属原子只能被氧化,但是对于处于中间态的金属阳离子,例如亚铁离子既具有还原性也具有氧化性,故A错误;汞为金属单质,但是在常温下是液体,所以金属单质在常温下不一定都是固体,故B错误;含金属元素的离子不一定都是阳离子,例如,MnO4-含有金属元素,但是是阴离子,故C错误;金属阳离子被还原不一定得到金属单质,例如铁离子可以被还原为亚铁离子,故D正确,为本题的答案。
点评:本题考查了金属的性质,该考点是高考考查的重点和难度,本题难度适中,有利于考查学生
本题难度:一般
2、实验题 黄铜矿(CuFeS2)是炼钢和炼铜的主要原料.在高温下灼烧生成二氰化二铁和氧化铜。三氧化二铁和氧化亚铜都是红色粉末.常用作颜料。某学校化学兴趣小组通过实验米探究一红色粉末是Fe2O3、Cu2O或两者的混合物。探究过程如下:
【查阅资料】Cu2O是一种碱性氧化物.溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO。
【提出假设】
假设1:红色粉末是Fe2O3。假设2:红色粉末是Cu2O。假设3:红色粉末是Fe2O3和Cu2O的混合物。
【设计探究实验】
取少量粉末放入足量稀硫酸中.在所得溶液中再滴加KSCN试剂。
(1)若假设1成立,则实验现象是???????。
(2)滴加KSCN试剂后溶液不变红色.某同学认为原同体粉末中一定不含三氧化二铁。你认为这种说法合理吗????。简述你的理由(不需写出反应的化学方程式):??????????????。
(3)若固体粉末未完全溶解,仍然有固体存在.滴加KSCN试剂时溶液不变红色.则证明原固体粉末是???,写出发生的氧化还原反应的离子方程式:?????。
【探究延伸】
(4)经过实验分析.确定红色粉末为Fe2O3和Cu2O的混合物。实验小组欲利用该红色粉末制取较纯净的胆矾(CuSO4・5H2O)。经过查阅资料得知.在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:

实验小组设汁如下实验方案:
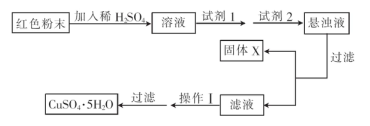
①试剂1为???.试剂2为???????. (填字母)
A.氯水
B.H2O2
C.NaOH
D.CuO
②固体X的化学式为????????。
③操作II为??????????????。
参考答案:(1)固体完全溶解,溶液呈血红色
(2)不合理;当原固
本题解析:
试题分析:(1)取少量粉末放入足量稀硫酸中.Fe2O3与硫酸发生反应:Fe2O3+3H2SO4=Fe2(SO4)3+H2O.反应后产生了Fe3+。在所得溶液中再滴加KSCN试剂,会看到固体完全溶解,溶液呈血红色。(2)滴加KSCN试剂后溶液不变红色.某同学认为原同体粉末中一定不含三氧化二铁。这种说法是错误的,因为当原固体粉末为Fe2O3和Cu2O的混合物时,加入稀H2SO4后产生的Fe3+与Cu反应生成Fe2+,滴加KSCN溶液后也可能不变红色。(3)若固体粉末未完全溶解,仍然有固体存在.滴加KS
本题难度:一般
3、选择题 在火星上工作的美国“勇气号”、“机遇号”探测车的一个重要任务就是收集有关Fe2O3及其硫酸盐的信息,用以证明火星上存在或曾经存在过水,以下叙述正确的是
A.Fe2O3与Fe3O4互为同素异形体
B.检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤 →向滤液中滴加KSCN溶液
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.明矾属硫酸盐,含结晶水,是混合物
参考答案:C
本题解析:
正确答案:C
A.不正确,Fe2O3与Fe3O4不互为同素异形体,它们不是单质。
B.不正确,步骤为:样品→粉碎→加稀盐酸溶解→过滤 →向滤液中滴加KSCN溶液
C.正确,除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.不正确,明矾属硫酸盐,含结晶水,但组成成分只有一种,不是混合物,是纯净物。
本题难度:一般
4、选择题 将mg Al2O3、Fe2O3的混和物溶解在过量的100mLpH值为1的硫酸中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好全部转化成沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为
A.0.1mol/L
B.0.05mol/L
C.0.2mol/L
D.无法计算
参考答案:A
本题解析:
依题意,混合物发生反应前后,反应物和生成物的关系如下:Al2O3+Fe2O3+H2SO4+NaOH Al(OH)3+Fe(OH)3+Na2SO4,易知最终溶液中NaOH全部转化为Na2SO4,根据H2SO4的量可以推算出NaOH的量来。n(H2SO4)=
Al(OH)3+Fe(OH)3+Na2SO4,易知最终溶液中NaOH全部转化为Na2SO4,根据H2SO4的量可以推算出NaOH的量来。n(H2SO4)= 本题难度:一般
本题难度:一般
5、选择题 将两种金属单质组成的混合物11克加到足量的稀H2SO4中,最终可得到11.2升H2(标况下),则这两种金属可能是
A.Zn和Fe
B.Ag和Mg
C.Al和Cu
D.Mg和Zn
参考答案:C
本题解析:n(H2)=0.5mol,反应转移1mol电子,金属质量11g,混合物中一种金属质量大于11g转移1mol电子,一种金属质量小于11g转移1mol电子。转移1mol电子所需金属质量:锌-32.5g;铁-28g;银-无穷大;镁-12g;铝-9g。选项中C符合。
点评:金属置换氢的相关计算。
本题难度:简单