微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (9分)为测定碳酸钙纯度(设所含杂质为SiO2),同学们设计了如下两个实验方案:
【方案I】
(1)组装发生并测定生成气体体积的实验装置,并检验气密性;
(2)称取碳酸钙样品W g;
(3)加入过量盐酸;
(4)收集并测定生成的气体体积V mL。
问题I―1:如果称量样品时,砝码底部有一处未被实验者发现的残缺,那么测定的碳酸
钙的纯度会????????(填“偏高、偏低、无影响”)。
问题I―2:在方框中画出测定生成的气体体积的装置简图。

【方案II】
(1)称取碳酸钙样品Wg;
(2)在锥形瓶中用C mol/L盐酸V mL(过量)溶解样品;
(3)加入甲基橙作指示剂,再用浓度为C1 mol/L的标准氢氧化钠溶液滴定过量的盐酸,用去氢氧化钠溶液V1毫升。(已知甲基橙的变色范围是pH=3.1~4.4)
问题II―1:未滤去不溶物SiO2,对测定结果是否有影响?(填有或无)?????????;
理由是?????????????????????????????????????????????。
问题II―2:碳酸钙纯度表达式?????????????????????????????????????????。
【方案评价】
你认为以上两个方案中,最好的方案是???????????????????,
另一个方案不够好的理由是????????????????????????????????????????????。
2、选择题 实验室用自来水制取蒸馏水的方法是[???? ]
A.过滤
B.蒸馏
C.萃取
D.分液
3、实验题 已知粗盐中含有CaCl2、MgCl2及一些可溶性硫酸盐,请根据你所学的知识,将除杂试剂、所除杂质以及除杂时的化学方程式按照除杂顺序填入下表:
试剂加入顺序
| 加入的试剂
| 所除杂质
| 化学方程式
|
①
| ?
| ?
| ?
|
②
| ?
| ?
| ?
|
③
| ?
| ?
| ?
|
④
| ?
| ?
| ?
4、选择题 要将含有杂质的工业乙醇提纯,通常采用的方法是
A.蒸馏
B.重结晶
C.过滤
D.萃取
5、实验题 (10分)欲用含有少量氯化钙的氯化钠固体,配制100 mL 1mol/L的氯化钠溶液,设计了下面的操作方案。根据方案操作步骤回答下列问题:
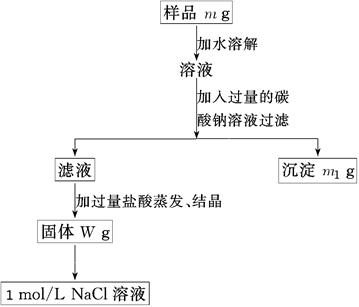
⑴称量粗盐样品m g,样品放在托盘天平左盘上。
⑵过滤时,需用到的玻璃仪器除烧杯、玻璃棒外有????????????????????????。
⑶蒸发操作时应将液体放在___???????___中加热,等加热至____??????____时即停止加热。
⑷在样品的溶液中加入过量的Na2CO3溶液,作用是____________________________,反应的离子方程式是___?????????????????????????????___________________。
⑸在滤液中加入盐酸的作用是________?????????????????????________,发生反应的化学方程式是____???????????????????????????????????????_______。
⑹配制100 mL 1mol/L的NaCl溶液时,应从W g固体中称取NaCl的质量为____________。
|