微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 美国亚利桑那州大学(ASU)和阿贡国家实验室的科学家最近设计出生产氢气的人造树叶,原理为:2H2O(g)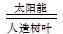 2H2(g)+O2(g)。有关该反应的说法正确的是
2H2(g)+O2(g)。有关该反应的说法正确的是
A.△H <0????????????????????????????
B.△S <0???????
C.化学能转变为电能????????????????????
D.氢能是理想的绿色能源
参考答案:D
本题解析:
试题分析:该反应为水的分解反应,属于吸热反应,即△H>0;正反应属于熵增,即△S>0;该反应实现了太阳能转化为化学能;氢能属于绿色能源;综上可确定D项正确。
本题难度:一般
2、选择题 用A、B、C来表示某三种元素符号,已知A2 + 2C-=2A- + C2,B2 + 2A-=2B- + A2,这两个反应都能从左向右进行,则反应C2 + 2B-=2C- + B2进行的方向是
A.从左向右?????????????????? B.从右向左??????????? C.先向左后向右???? D.无法判断
参考答案:B
本题解析:略
本题难度:简单
3、填空题 煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃
| 400
| 500
| 800
|
平衡常数K
| 9.94
| 9
| 1
试回答下列问题
⑴上述正向反应是????????反应(填“放热”或“吸热”)。
⑵在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有??????????(选填A、B、C、D、E)。
?
| n(CO)
| n(H2O)
| n(H2)
| n(CO2)
| A
| 1
| 5
| 2
| 3
| B
| 2
| 2
| 1
| 1
| C
| 3
| 3
| 0
| 0
| D
| 0.5
| 2
| 1
| 1
| E
| 3
| 1
| 2
| 1
⑶已知在一定温度下:
C(s)+CO2(g) 2CO(g)平衡常数K; 2CO(g)平衡常数K;
C(s)+H2O(g) CO(g)+H2(g)?平衡常数K1; CO(g)+H2(g)?平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g)平衡常数K2; H2(g)+CO2(g)平衡常数K2;
则K、K1、K2之间的关系是K=???????????。
⑷若在500℃时进行,设起始时CO和H2O的起始浓度均为0.010mol/L,在该条件下,CO的平衡转化率为:??????????。
⑸若反应在800℃进行,设起始时CO(g)和H2O(g)共为1mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=????????。
参考答案:⑴放热??⑵BCD???⑶K1/K2??⑷75%?⑸X
本题解析:
试题分析:(1)根据表中数据可知,随着温度的升高,平衡常数减小,说明升高温度平衡向逆反应方向移动,所以正方应是放热反应。
(2)由于反应前后体积不变,所以设容器的容积是1L,则ABCD中 的比值分别是 的比值分别是 本题难度:一般 本题难度:一般
4、选择题 298K下,将1mol蔗糖溶解在1L水中,此溶解过程中体系的?G = ?H-T?S和?S的变化情况是
A.?G>0,?S<0
B.?G<0,?S>0
C.?G>0,?S>0
D.?G<0,?S<0
参考答案:B
本题解析:蔗糖溶解是熵值增加的,即?S>0,过程自发,说明溶解放热,所以选项B正确。
本题难度:一般
5、选择题 一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g)  ?C(g)+D(g),当下列物理量不发生变化时,能表明该反应一定达到平衡状态的是(??) ?C(g)+D(g),当下列物理量不发生变化时,能表明该反应一定达到平衡状态的是(??)
A.A的物质的量浓度
B.混合气体的总物质的量
C.容器内气体的压强
D.混合气体的密度
参考答案:D
本题解析:
试题分析:A项错误,物质A为固体,其物质的量浓度始终为0;B项错误,混合气体的总物质的量从反应开始一直保持不变;C项错误,可逆反应两边的气体压强始终相同,容器内气体的压强也始终相同,不能表明该反应达到平衡状态。当容器中混合气体的密度保持不变是,表明该反应一定达到平衡状态,选项D正确。
点评:化学反应速率平衡为高考重要考点,全面的要求考生对可逆反应、化学反应速率平衡等的理解与熟练掌握,具有一定的分析力度与考查难度,考生平时应当多注重化学反应速率平衡相关知识的实践练习。
本题难度:简单
|
|