微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 向Cu和Cu2O的混合物27.2g中加入某浓度的硝酸0.1L,固体物质完全反应,生成NO2、 N2O4、NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,溶液恰好呈中性,金属离子也已完全沉淀,沉淀质量为39.2g。以下所得结论不合理的是
A.硝酸的物质的量浓度为12.0mol/L
B.产生的气体在标准状况下的体积为13.44L
C.Cu与Cu2O 的物质的量之比为2:1
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
参考答案:AB
本题解析:
试题分析:在所得溶液中加入1.0mol/L?的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,溶液中溶质为NaNO3,n(NaNO3)=n(NaOH)=1.0mol/L×1.0L=1mol,沉淀为Cu(OH)2,质量为39.2g,物质的量为39.2g÷98g/mol=0.4mol,根据铜元素守恒有n(Cu)+2n(Cu2O)=n[Cu(OH)2],所以反应后的溶液中n[[Cu(NO3)2]=n[Cu(OH)2]=0.4mol,故反应中硝酸有剩余。A、混合气体中N2O4的含量不确定,不能确
本题难度:一般
2、填空题 如图为配制250mL0.2mol/LNa2CO3溶液的示意图.
回答下列问题:
(1)选择容量瓶的规格是______.
(2)①中称得Na2CO3______g.
(3)玻璃棒在②、③两步中的作用分别是______、______.
(4)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”、“偏低”或“无影响”)
A.某同学在第⑧步观察液面时仰视______;
B.没有进行操作步骤④和⑤______;
C.在第⑤步不慎有少量液体流到容量瓶外______;
D.在步骤④中,药品放在右盘,砝码放在左盘(使用游码)______.

参考答案:(1)选取容量瓶的规格应该等于或稍微大于配制溶液的体积,所以
本题解析:
本题难度:一般
3、选择题 .NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A.标准状况下,2.24LH2O含有的电子数等于NA
B.常温下,100mL 1mol・L-1Na2CO3溶液中阴离子总数小于0.1NA
C.标准状况下,分子数为NA的N2、C2H4混合气体体积约为22.4L,质量为28g
D.3.4gNH3中含N―H键数目为0.2NA
参考答案:C
本题解析:标准状况下,水不是气体,不能适用于气体摩尔体积;碳酸钠溶于水发生水解,生成碳酸氢钠和氢氧化钠,所以阴离子个数是大于0.1NA;氮气和乙烯的相对分子质量都是28,所以选项C正确;3.4g氨气是0.2mol,含有含N―H键数目为0.6NA,因此答案选C。
本题难度:困难
4、选择题 在0℃和101 kPa的条件下,将4.00 g氩气、1.40 g氮气和1.60 g氧气混合,该混合气体的密度是相同条件下氢气密度的(??? )
A.35倍
B.17.5倍
C.7倍
D.14倍
参考答案:B
本题解析:三种气体的物质的量分别是0.1mol、0.05mol和0.05mol,则混合气的平均相对分子质量是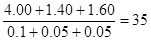 。由于在等温等压时,气体的密度之比是相应的摩尔质量之比,因此混合气的密度是相同条件下氢气密度的35÷17.5倍,答案选B。
。由于在等温等压时,气体的密度之比是相应的摩尔质量之比,因此混合气的密度是相同条件下氢气密度的35÷17.5倍,答案选B。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是(相对原子质量:D-2? O-16? Cu-64)
A.18 g的D216O中含有的中子数为9 NA
B.物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA
C.33.6 L NO2溶于足量的水得到的溶液中含有的NO3-数为NA
D.32 g铜发生氧化还原反应,一定失去NA个电子
参考答案:A
本题解析:
试题分析:A、18 g的D216O的物质的量是18g/20g/mol,1个D216O中含有的中子数为8+2=10个,所以18 g的D216O中含有的中子数为18g/20g/mol×10="9" NA,正确;B、未给出溶液体积,无法计算溶液中含有的氧原子数,错误;C、未指明标准状况,所以33.6 L NO2的物质的量无法计算,溶液中含有的NO3-数无法计算,错误;D、32 g铜的物质的量是0.5mol,发生反应时Cu失去的电子数未知,可能失去1个电子,也可能失去2个电子,所以0.5mol的Cu失去的
本题难度:简单