微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 将56 g铁粉和16 g硫粉隔绝空气加热,使其充分反应并冷却后,再加入适量盐酸,最后可得气体体积为(标准状况)
A.5.6 L
B.11.2 L
C.22.4 L
D.44.8 L
参考答案:C
本题解析:略
本题难度:简单
2、选择题 下列有关实验现象和解释或结论都正确的是
选项
| 实验操作
| 实验现象
| 解释或结论
|
A
| 将充满NO2的密闭玻璃球浸泡在热水中
| ?红棕色变深
| ?反应2NO2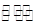 N2O4的 N2O4的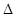 H<0 H<0
|
B
| 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡
| 下层分别呈无色???和紫红色
| ??还原性:I->Br->Fe2+
|
C
| 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水
| 有白色沉淀出现
| ???该钾盐是K2CO3
|
D
| ???把SO2通入紫色石蕊试液中
| ???紫色褪去
| ??? SO2具有漂白性
参考答案:A
本题解析:
试题分析:A、将充满NO2的密闭玻璃球浸泡在热水中,红棕色变深,说明升高温度反应2NO2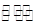 N2O4平衡逆向移动,△H<0,正确;B、将少量的溴水分别滴入FeCl2溶液、NaI溶液中,发生的反应分别为Br2 + 2Fe2+====2Fe3+ + 2Br-、Cl2 + 2I- ====2Cl- + I2 N2O4平衡逆向移动,△H<0,正确;B、将少量的溴水分别滴入FeCl2溶液、NaI溶液中,发生的反应分别为Br2 + 2Fe2+====2Fe3+ + 2Br-、Cl2 + 2I- ====2Cl- + I2
本题难度:一般
3、计算题 (6分)将3.2 g Cu与足量的浓硫酸在加热条件下充分反应。
(1)其中被还原的硫酸的物质的量为???????????????????。
(2)把反应后的溶液稀释至500 mL,取出50 mL,向其中加入足量的BaCl2溶液,得到沉淀20.97 g,则稀释后所得溶液中SO42-的物质的量浓度为?????????????????。
(3)若浓硫酸中含溶质为b mol,投入足量的铜片并加热,充分反应后,被还原的硫酸的物质的量n (H2SO4)????????????0.5 b mol(填“>”、“<”或“=”)。
参考答案:(6分)(1)0.05mol?????????? (2) 1
本题解析:
答案:(1)0.05mol?????????? (2) 1.8mol/L?????????? (3) <
解析:3.2 g Cu为0.05mol
由方程式Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O可知: CuSO4+SO2↑+2H2O可知:
(1)??????其中被还原的硫酸的物质的量为0.05mol,与被还原
本题难度:简单
4、选择题 下列措施不合理的是
A.用SO2漂白纸浆和草帽辫
B.用硫酸清洗锅炉中的水垢
C.高温下用焦炭还原SiO2制取粗硅
D.用Na2S作沉淀剂,除去废水中的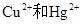
参考答案:B
本题解析:
试题分析:
A.利用二氧化硫的漂白性,正确;B.水垢的成分是碳酸钙和氢氧化镁,而硫酸钙是微溶的,所以不能用硫酸除水垢,而应作盐酸或醋酸;错误;C.SiO2 + 2C =(高温)Si +2CO↑ ;正确;D.CuS、HgS均是难溶物,故正确。
本题难度:一般
5、选择题 下图所示的是验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。将硫酸滴入装有亚硫酸钠固体的培养皿中。
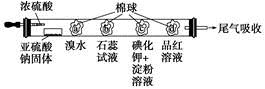
关于此实验的“现象”、“解释或结论”以及对应关系均正确的是
选项
| 现象
| 解释或结论
| A
| a处黄色褪去
| 非金属性:Br>S
| B
| b处变为红色
| 二氧化硫与水反应生成酸性物质
| C
| c处变为蓝色
| 二氧化硫具有一定的氧化性
| D
| d处红色先褪去后恢复
| 二氧化硫具有漂白性且漂白性不稳定
?
参考答案:B
本题解析:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O。a处反应为SO2+Br2+H2O=H2SO4+2HBr,证明SO2的还原性大于Br-,而不是非金属性Br>S,A错误;b处反应为SO2+H2O H2SO3 H2SO3 本题难度:一般 本题难度:一般
|
|