��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1���ƶ��� A��B��C��D��E��ԭ������������������ֶ�����Ԫ�ء�B��Eͬ���壬��������������ϼۣ�������ϼۣ�0��A��C��D��C֮�䶼���γ�ԭ�Ӹ����ȷֱ�Ϊ2��1��1��1�����ֻ�����Խ�������й����⡣
(1)��A2C2�����к��еĻ�ѧ����________��________��
(2)C��D�γɵĻ�����ĵ���ʽΪ? ___________________________��
(3)ʵ���ҿ�����B��C��D��ɵĻ�����Ϊ��Ӧ��֮һ��ȡ��A��C��D��ɵĻ������Ӧ�Ļ�ѧ����ʽΪ?_________________________________________��
(4)д��E������A��C��D�γɵĻ������ˮ��Һ��Ӧ�����ӷ���ʽ_________________________________________��
2������� ��֪��A��B��C��D����Ԫ�ص���������С��18�����ǵĺ˵����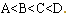 ��A��B�����ɻ�����AB2��ÿ��AB2�����к���22�����ӣ�CԪ��ԭ�ӵĴ���������Ϊ������������2����DԪ��ԭ�ӵ������������ȴ������1�������Ԫ�ط��ŷֱ�Ϊ��A__________��B__________��C____ ______��D_________��
��A��B�����ɻ�����AB2��ÿ��AB2�����к���22�����ӣ�CԪ��ԭ�ӵĴ���������Ϊ������������2����DԪ��ԭ�ӵ������������ȴ������1�������Ԫ�ط��ŷֱ�Ϊ��A__________��B__________��C____ ______��D_________��
3��ѡ���� ���ǵ������ڢ�A��Ԫ�أ������������ڱ��е�λ�����У��鲻���ܾ��е�������
A.��ĵ�����ͨ��������ǹ���
B.As2O5��ˮ������һ��ǿ��
C.AsH3��PH3�ȶ�
D.��ij������ϼ���-3��+3��+5
4������� ��ѧ������ȵķ�����Ԥ���������ʵ����ʣ������H2+Cl2�T2HCl���Ʋ⣺H2+Br2�T2HBr�����������Եģ������2Na2O2+2CO2�T2Na2CO3+O2����2Na2O2+2SO2�T2Na2SO3+O2�Ǵ���ģ�Ӧ��ΪNa2O2+SO2�TNa2SO4��
��1�����и����������ȷ��Ϊ______��
A����Ԫ�����ڱ���Al��GeԪ�ص������ԣ��Ʋ�ƣ�Ca��Ԫ����﨣�Rb��Ԫ����������
B����NH4Cl�TNH3��+HCl���Ʋ�NH4I�TNH3��+HI��
C����2CO2+Ca��ClO��2+2H2O�TCa��HCO3��2+2HClO�Ʋ�CO2+NaClO+H2O�TNaHCO3+HClO
D����Fe3O4+8HCl�TFeCl2+2FeCl3+4H2O�Ʋ�Pb3O4��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��Pb3O4+8HCl��Ũ���T2PbCl2+PbCl4+4H2O
��2��������������NԪ�ش���OԪ�ص���ʵ���Ʋ�����ϵ������ǵĽṹ��ʽ[CH2OH��CHOH��4CHO]��������ӦΪ______��
��3����2F2+2H2O�T4HF+O2��ӦԤ��2F2+4NaOH�T4NaF+2H2O+O2��Ȼ����ʵ�飬��ij�����£����ʵ�����ȵ�F2��NaOHǡ����ȫ��Ӧ�����ɷ����ơ�ˮ��һ�����壬�����ʵ����д����Ӧ�Ļ�ѧ����ʽ______��
5��ѡ���� ����������ȷ���ǣ�������
A��ͬһ����Ԫ�ص�ԭ�ӣ��뾶ԽСԽ����ʧȥ����
B��ͬһ�����Ԫ�أ�ԭ�Ӱ뾶Խ��������Խǿ
C����A��Ԫ���γɵĵ��ʣ����۵���Ԫ��ԭ���������������
D�����ϵ��£���A��Ԫ���γɵ��⻯���ȶ�������