��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��°��������ҹ����������Ļ���ר�ң������Ƽ���������ش��ף����������������Ƽ�����������Ƽ������ͼ����ʵ������ģ�⡰�����Ƽ������ȡ̼������һ����ʵ��װ�ã�ʵ�鲽��Ϊ��
�����Ӻ�װ�ã����������ԣ���������װ��ҩƷ��
���ȴ�D�ķ�Һ©������������Ũ��ˮ��ֱ�����������岻������C�еı���NaCl��Һ���ܽ�ʱ����ͨ��A�в��������壮Ƭ�̺��ձ���������ɫ���壨̼�����ƣ���������C��ͨ���������壬ֱ�������й������Ϊֹ��
�۹����ձ������õĻ����õ�̼�����ƹ��壮
������Һ�м����������Ȼ��ƹ��壬������Ӧ��
NaCl��s��+NH4Cl��aq��=NaCl��aq��+NH4Cl��s�����������ˣ��˳�����������ʣ�
����Һ��ע���ձ�C�У��ظ�ʹ�ã�������һ���Ʊ���
�Իش��������⣺
��1������װ��A�����Եķ�����______��
��2���ձ�C�з�����Ӧ�Ļ�ѧ����ʽΪ______��
��3��A�г�ѡ�õĹ���Ϊ______��B��Ӧѡ�õ�Һ��Ϊ______��
��4��������б�������D�з�����Ӧ���������������A�з�����Ӧ�������壬ԭ����______��
��5����������ڽϸ��¶ȣ���60�棩�»����ڽϵ��¶��£���0�桫10�棩�½��к��ʣ�______����ϸߡ��ϵ͡���
��6������������õ��Ȼ�茶����г������������Ȼ��ƺ�̼�����ƣ�Լռ5%��8%��������Ƽ�ʵ��֤�����ù���ijɷִ����Ȼ�泥���Ҫд����������������ͽ��ۣ�______��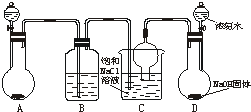
�ο��𰸣���1������װ�������ԣ���Ҫ������װ���ڵ�ѹǿ�仯���жϣ�����
���������
�����Ѷȣ�һ��
2��ʵ���� ��һ��(4��)�����е����������ʣ�д����ȥ��Щ���ʵ��Լ���
��1��MgO (Al2O3) ???????????????��2��Cl2(HCl)???????????
��3��FeCl3(FeCl2)???????????????��4��NaHCO3��Һ(Na2CO3)??????????
������(6��)��ˮ�к��д������Ȼ�þ���Ӻ�ˮ����ȡþ��������������ͼ��ʾ��
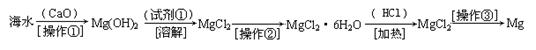
�ش��������⣺
д���ں�ˮ�м�������������������þ�Ļ�ѧ����ʽ????????????????????��
��������Ҫ��ָ???????���Լ��ٿ�ѡ��?????????��
��������ָ??????????�������������տɵý���þ��
��������8�֣�ʵ��������480ml 0��1mol��L-1��Na2CO3��Һ���ش��������⣺
��1��Ӧ��������ƽ��ȡʮˮ̼���ƾ���????????g��
��2����ͼ��ʾ������������Һ�϶�����Ҫ����??????(�����)����ʵ�����貣������E���Ϊ???????mL��
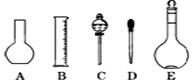
��3������ƿ�ϱ��У����¶ȡ���Ũ�ȡ�����������ѹǿ���ݿ̶��ߡ�����ʽ���ʽ�������е�????????���������ַ��ţ�
��4�������������Ҫ�����ǣ�a����ƿ��b�ձ���c��ͷ�ιܡ�d������ƽ�������ڲ���������ʹ�õ�ǰ��˳����???????������д��ĸ��ÿ������ֻ��ѡ��һ�Σ�
��5���������ǻ�ѧʵ���г��õ�һ�ֲ������ߣ�����������Һ�Ĺ����в�����������??????����;������д���֣�
��6����ʵ��ʱ���������������ʹ��Һ��Ũ��ƫ�͵���???????��
A������ǰû�н�����ƿ�е�ˮ������
B��̼����ʧȥ�˲��ֽᾧˮ��
C��̼���ƾ��岻�������л����Ȼ��ƣ�
D������̼���ƾ���ʱ�����������⣻
E������ʱ���ӿ̶���
�ο��𰸣���һ����4�֣���1�� NaOH��Һ��2������NaCl��Һ��3
���������
�����������һ����1������Al2O3Ϊ�������������NaOH��Һ�ɳ�ȥMgO�е�Al2O3���ʡ�
��2��Cl2�ڱ���NaCl��Һ�е��ܽ�Ⱥ�С�������ñ���NaCl��Һ�ɳ�ȥCl2�е�HCl��
��3��Cl2�ɰ�FeCl2����ΪFeCl3������ͨ��Cl2�ɳ�ȥFeCl2��
��4��CO2��H2O��Na2CO3��Ӧ����NaHCO3������CO2�ɳ�ȥNaHCO3�е�Na2CO3���ʡ�
����������CaO��H2O��Ӧ����Ca(OH)2��CaO+H2O=Ca(OH)2��Ȼ��Ca(OH)2��MgCl2��Ӧ����Mg(OH)2��Ca(OH)2+MgCl2=Mg(OH)2+CaCl2���ӺͿɵ��ܷ���ʽ��CaO+H2O+MgCl2=Mg(OH)2+CaCl2�������ٰ�Mg(OH)2�������������Ϊ���ˣ��Լ�����Mg(OH)2��Ӧ����MgCl2��ΪHCl���������Ǵ�MgCl2��Һ�еõ�MgCl2��6H2O��Ϊ����Ũ������ȴ�ᾧ�����ˡ�
��������1������480ml��Ҫѡ��500ml����ƿ��m(Na2CO3��10H2O)=0��5L��0��1mol/L��286g/mol=14��3g��
��2������һ�����ʵ���Ũ�ȵ���Һ���ò�����ƿ����Һ©������������ƿ�Ĺ��ʵ����������ƿΪ500ml��
��3������ƿ�ϱ����¶ȡ������Ϳ̶��ߣ��ʴ�Ϊ�٢ۢݡ�
��4��������������ƽ�������ʣ�Ȼ������ʷ����ձ��У���ˮ�ܽ⣬����Һע������ƿ������ý�ͷ�ιܶ��ݣ������ڲ���������ʹ�õ�ǰ��˳����dbac��
��5���ܽ�����ʱ�ò��������裬ת����Һʱ�ò��������������Բ�����������2����;��
��6��A�� ����ǰû�н�����ƿ�е�ˮ��������Ũ����Ӱ�죻B��̼����ʧȥ�˲��ֽᾧˮ��Na2CO3���Ũ��ƫ�ߣ�C��̼���ƾ��岻�������л����Ȼ��ƣ�������Na2CO3���٣�Ũ��ƫ�ͣ�D������̼���ƾ���ʱ�����������⣬������Na2CO3�������Ũ��ƫ�ߣ�E������ʱ���ӿ̶��ߣ�ʹ��Һ��������Ũ��ƫ�͡�
�����Ѷȣ�һ��
3��ѡ���� ʵ�����о���ѧ�Ļ�������ͼ����ʾ��ʵ�鷽����װ�û������ȫ��ȷ����[???? ]
A.
B.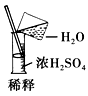
C.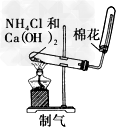
D.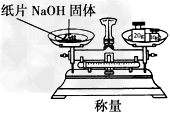
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ����ʵ�������Ҫ�¶ȼ��Ҳ���������Һ���е���
A���Ҵ�����ϩ
B������������
C�������屽
D��ʵ��������ʯ��
�ο��𰸣�D
�����������
�����Ѷȣ���
5��ѡ���� ���в����������
A������0��1mol��L-1��H2SO4��Һʱ����ȡŨ����С��ע��ʢ����������ˮ������ƿ��
B����Ҫ��ȥCO2�к��е�����SO2���壬��ͨ��ʢ�б���NaHCO3��Һ��ϴ��ƿ
C����ʵ������ʹ�ý�����ʱ�������Ż𣬿�������ϸɳ���
D������ҺpHʱ�����øɾ��IJ�����պȡ��Һ�ε����ڱ������ϵ�pH��ֽ��
�ο��𰸣�A
���������
���������A������ȷ������ƿ��������ϡ��Ũ���ᣬŨ����Ӧ���ձ���ϡ�Ͳ���ȴ��ת��������ƿ��B����ȷ��SO2��HCO3�D=Cl2��HSO3�D��C����ȷ����ϸɳ���������������D����ȷ������ҺpHʱ�����øɾ��IJ�����պȡ��Һ�ε����ڱ�������Ƭ���ϵ�pH��ֽ�ϣ�ע��pH��ֽ������ˮʪ��ѡA��
�����Ѷȣ���