��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��װ���У����ܷ���ԭ��ط�Ӧ����
�ο��𰸣�D
���������
������ԭ��صĹ��������������Բ�ͬ�������缫���������Һ���պϻ�·���Է���������ԭ��Ӧ��
�⣺ǰ����װ�þ�����ԭ��صĹ��������������Բ�ͬ�������缫���������Һ���պϻ�·���Է���������ԭ��Ӧ���ڵ��ĸ�װ���У������γɱպϻ�·��
��ѡD��
�����Ѷȣ�һ��
2��ѡ���� ��A��B��C��D�Ŀ����Ƭ����������ʵ�飬
��A��B�õ���������ͬʱ����ϡH2SO4�У�A��Ϊ����
��C��D�õ���������ͬʱ����ϡH2SO4�У�������C�����ߡ�D
��A��C������ͬʱ����ϡH2SO4��C��������������
��B��D������ͬʱ����ϡH2SO4�У�D������������Ӧ
�����ֽ����Ļ��˳��Ϊ[???? ]
A��A>B>C>D
B��C>A>B>D
C��A>C>D>B
D��B>D>C>A
�ο��𰸣�C
���������
�����Ѷȣ�һ��
3��ѡ���� ��ͼΪ���ѵ�أ�����˵����ȷ����

A��һ��ʱ ���пƬ�������С
���пƬ�������С
B��ͭ�缫�����������ɫ
C��������ͭͨ����������п
D��п�缫�Ǹõ�ص�����
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ��ʾ�����缫һΪ̼����һΪ��Ƭ������������ָ�뷢��ƫת����a�����д����������ɣ�������������ȷ���ǣ�������
A��aΪ����������Ƭ���ձ��е���ҺΪ����
B��bΪ����������Ƭ���ձ��е���ҺΪ����ͭ��Һ
C��aΪ��������̼�����ձ��е���ҺΪ����
D��bΪ��������̼�����ձ��е���ҺΪ����ͭ��Һ
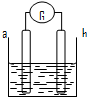
�ο��𰸣�A��a�����д����������ɣ�˵��a��������Ӧ����̼��������b��
���������
�����Ѷȣ���
5��ѡ���� ���������վñ������ڣ�����������Ag2S��Ե�ʣ����ݵ绯ѧԭ���ɽ������´����������������м���ʳ����Һ���ٽ���ڵ������������Һ�У�һ��ʱ����ֺ�ɫ����ȥ������˵����ȷ���ǣ�������
A����������������һֱ���ֺ���
B������Ϊ������Ag2S����ԭ���ɵ�����
C���ù������ܷ�ӦΪ2Al+3Ag2S�T6Ag+Al2S3
D����ɫ��ȥ��ԭ���Ǻ�ɫAg2Sת��Ϊ��ɫAgCl
�ο��𰸣�A�������������������У��������Ļ����Դ�����������Ϊ������ʧ
���������
�����Ѷȣ�һ��