微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
Ni(OH)2 + M =" NiOOH" + MH
已知:6NiOOH + NH3 + H2O + OH-="6" Ni(OH)2 + NO2-
下列说法正确的是
NiMH 电池放电过程中,正极的电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH-
充电过程中OH-离子从阳极向阴极迁移
充电过程中阴极的电极反应式:H2O + M + e-=" MH" + OH-,H2O中的H被M还原
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
参考答案:A
本题解析:
试题分析:B.充电过程中阴离子OH-离子向阳极迁移,不正确;C. H2O + M + e-=" MH" + OH-,H2O中的H电离成H+得到电子被还原;D. 由已知可知NiOOH 与NH3发生反应。A为阿伏加德罗常数的值来表示微粒数目。
本题难度:一般
2、实验题 2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200oC左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。电池总反应为:C2H5OH +3O2 =2CO2 +3H2O,电池示意如图:
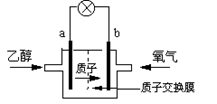
(1)_________极(填a或b)为电池的负极,电池工作时电流方向为______________;
(2)写出电池正极反应方程式___________________;
(3)电池工作时,1mol乙醇被氧化时就有________mol电子转移。
参考答案:
(1)a极为电池的负极,电流由b极沿导线到a极
本题解析:略
本题难度:简单
3、选择题 锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。 某种锂电池的总反应式是Li+MnO2= LiMnO2。下列说法正确的是
A.Li是负极,电极反应为Li-e-=Li+
B.Li是正极,电极反应为Li+e-=Li-
C.MnO2是负极,电极反应为MnO2+e-=MnO2-
D.锂电池工作过程:化学能转化为电能
参考答案:AD
本题解析:
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。所以根据方程式可知,Li是负极,失去电子,A正确,B不正确;二氧化锰是正极,得到电子,C不正确;原电池是把化学能转化为电能的注重,D正确,答案选AD。
点评:该题是高考中的常见题型,属于中等难度试题的考查,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生解题能力的培养和训练,旨在考查学生灵活运用原电池原理解决实际问题的能力,有利于培养学生
本题难度:简单
4、选择题 氢氧燃料电池是一种高性能电池,总反应为2 H2 + O2 =" 2" H2O,电解质溶液为KOH溶液,下列有关该电池的叙述中不正确的是( )。
A.H2为负极,O2为正极
B.负极反应:2H2 +4OH-→4H2O + 4e-
C.工作时电解质溶液的PH不断增大
D.正极反应:O2 + 4e- +2 H2O→4OH-
参考答案:
本题解析:略
本题难度:简单
5、填空题 (6分)铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42- 2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列问题(不考虑氢、氧的氧化还原)
(1)放电时:正极的电极反应式是 ;当外电路通过1mol电子时,电解液中消耗H2SO4 mol。
(2)充电时,Pb 和电源的 极相连,此时发生的电极反应式为 。
参考答案:(1)PbO2+2e-+4H++SO42-=PbSO4+2H
本题解析:(1)放电相当于原电池,在原电池中正极得到电子,根据反应式可知,二氧化铅得到电子,所以正极反应式为PbO2+2e-+4H++SO42-=PbSO4+2H2O。根据总反应式可知,每消耗2mol硫酸,反应中就转移2mol电子,所以如果通过1mol电子,则消耗1mol硫酸。
(2)充电相当于放电的逆反应,放电是铅是负极失去电子,所以充电时铅和电源的负极相连,作阴极,得到电子,所以反应式为PbSO4+2e-=Pb+SO42-。
本题难度:一般