微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于复合材料的说法不正确的是[???? ]
A、金属材料不能制成复合材料
B、玻璃钢是日常生活中常用的复合材料,其强度可超过合金钢
C、跳高运动员用的撑杆为复合材料制作
D、复合材料具有不可估量的应用前景,人类已从合成材料时代进入复合材料时代
参考答案:A
本题解析:
本题难度:简单
2、选择题 下列金属冶炼的反应原理,错误的是???
A.2NaCl(熔融) 2Na +Cl2↑
2Na +Cl2↑
B.MgO+H2 Mg+ H2O
Mg+ H2O
C.Fe3O4+4CO  3 Fe +4 CO2
3 Fe +4 CO2
D.2 HgO 2 Hg+ O2↑
2 Hg+ O2↑
参考答案:B
本题解析:
试题分析:特别活泼的金属用电解法冶炼,比较活泼的计算用热还原法冶炼,不活泼的金属用热分解法冶炼。Mg是活泼的计算,应该用电解熔融的MgCl2的方法冶炼,其余的方法正确。因此选项是B。
本题难度:一般
3、填空题 海洋是个巨大的资源宝库,海水资源的利用具有非常广阔的发展前景。海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下所示:
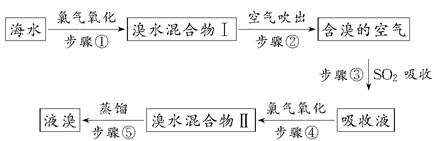
(1)步骤①反应的廊子方程式为_______________________________。
(2)步骤③反应的化学方程式为_________________________________。
(3)Br的原子序数是________,在周期表中位于第________周期、________族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:________________。
(5)为什么不直接用“溴水混合物Ⅰ”而要用“溴水混合物Ⅱ”进行蒸馏,得出液溴?
参考答案:(1)2Br-+Cl2=Br2+2Cl- (2)SO2+Br
本题解析:(1)Cl的非金属性大于Br,海水中含有的Br-被氯气置换,Cl2+2Br-=Br2+2Cl-。
(2)空气中的Br2与SO2反应,得到含高浓度Br-的溶液,SO2+2H2O+Br2=2HBr+H2SO4。
(3)溴为第四周期,ⅦA族元素;根据各周期元素的个数,计算第四周期稀有气体元素的原子序数,由此推出Br的原子序数=2+8+8+18-1=35。
(4)根据蒸馏分离原理进行回答。水的沸点为100℃,温度过高水蒸发量增大,温度过低,溴的挥发量减少,不能完全蒸出,回收率降低。
(5)
本题难度:一般
4、选择题 在航天飞机返回地球大气层时,为防止其与空气剧烈摩擦,产生高温(1000℃以上)而被烧毁,需在航天飞机外表面安装保护层.该保护层的材料可能是( )
A.铝合金
B.合成纤维
C.耐高温新型陶瓷
D.塑料
参考答案:C
本题解析:
本题难度:简单
5、填空题 从海水中提取金属镁的生产步骤有:①浓缩结晶,②加熟石灰,③加盐酸,④过滤,⑤熔融电解,正确的生产步骤是??_???????????????。
参考答案:②④③①⑤
本题解析:略
本题难度:简单