微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中有关物质的量浓度关系和计算不正确的是?????????????????????????????(???)
A.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(NaHCO3)
<c(CH3COONa)
B.已知25°C时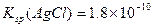 ,则在0.1mol・L-1AlCl3溶液中,Ag+的物质
,则在0.1mol・L-1AlCl3溶液中,Ag+的物质
的量浓度最大可达到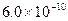 mol・L-1
mol・L-1
C.25°时,0.1mol・L-1Na2CO3溶液中水电离出来的OH-浓度大于0.1mol・L-1NaOH溶
液中水电离出来的OH-浓度
D.室温下,0.1mol・L-1NaHA溶液的pH=4,则有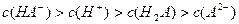
参考答案:D
本题解析:选项D,HA-是弱电解质离子,且HA-的电离大于水解,故应该是c(A2-)>c(H2A)。选项A,当pH相等时,原来碱性强的物质,浓度反而小;原来碱性弱的物质,浓度反而大;故选项A正确。选项B,根据c(Ag+)・c(C1―)=Ksp=1.8×10 -10,将c(Cl-)="0.3" mol.L-l代入式中计算即可。选项C,Na2CO3水解,促进水电离,NaOH是碱,抑制水电离。
本题难度:简单
2、选择题 13.9g XSO4・nH2O晶体,完全失水后,剩余7.6g粉末,若X的原子量为结晶水分子数的8倍,则X的原子量为
A.23
B.27
C.40
D.56
参考答案:D
本题解析:根据题意可知,结晶水的质量是13.9g-7.6g=6.3g,物质的量是0.35mol,所以有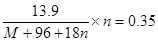 ,又因为8n=M,所以解得M=56,答案选D。
,又因为8n=M,所以解得M=56,答案选D。
本题难度:简单
3、选择题 现有CO、CO2、O3(臭氧)三种气体,下列叙述不正确的是
A.同温同压同体积时质量比为7:11:12
B.相同质量时所含氧原子的物质的量之比为1:2:3
C.标况下密度比为7:11:12
D.都含有1mol氧原子时则三种气体的物质的量之比为6∶3∶2
参考答案:B
本题解析:A 正确,同温同压同体积时质量比就是摩尔质量比28:44:48=7:11:12
B 错误相同质量时所含氧原子的物质的量之比为1/14 :1/11 :1/8
C 正确,标况下密度比为摩尔质量之比,所以是7:11:12
D 正确,假设都含有6摩尔氧原子,此时三种气体的物质的量之比为6∶3∶2
本题难度:简单
4、选择题 今有0.1mol/L Na2SO4溶液300mL,0.1mol/L MgSO4溶液200mL和0.1mol/L Al2(SO4)3溶液100mL,这三种溶液中硫酸根离子浓度之比是( )
A 1:1:1 B 3:2:1 C 3:2:3 D 1:1:3
参考答案:D
本题解析:
试题分析:0.1mol?L-1Na2SO4溶液中硫酸根离子浓度为0.1mol/L;0.1mol?L-1MgSO4溶液中硫酸根离子浓度为0.1mol/L;0.1mol?L-1Al2(SO4)3溶液中硫酸根离子浓度为0.3mol/L;所以三种溶液中硫酸根离子浓度之比为0.1mol/L:0.1mol/L:0.3mol/L=1:1:3,故D项正确。
考点:本题考查物质的量浓度的计算。
本题难度:一般
5、选择题 设NA为阿伏加德罗常数,下列说法中正确的是
A.标准状况下,密度为d g/L的某气体纯净物一个分子的质量为 g
g
B.常温常压下,17g甲基(―14CH3)所含的中子数为9NA
C.25℃时,1 L pH=13的NaOH溶液中含有NA个氢氧根离子
D.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子
参考答案:AD
本题解析:
试题分析:A、标准状况下,1mol气体的质量为:22.4dg,则一个分子的质量为 g,正确;B、1个―14CH3含8个中子,17g甲基(―14CH3)所含的中子数为:17g÷17g/mol×8NA=8NA,错误;C、1 L pH=13的NaOH溶液中含有0.1NA个氢氧根离子,错误;D、Na不论生成Na2
g,正确;B、1个―14CH3含8个中子,17g甲基(―14CH3)所含的中子数为:17g÷17g/mol×8NA=8NA,错误;C、1 L pH=13的NaOH溶液中含有0.1NA个氢氧根离子,错误;D、Na不论生成Na2
本题难度:一般