��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� (17��)�����仯�������ճ����������Ӧ�ù㷺���Ȼ���������ض��dz�����ˮ����������ͼΪ�Ʊ��Ȼ�������һ�������Ʊ�������صĹ������̡�
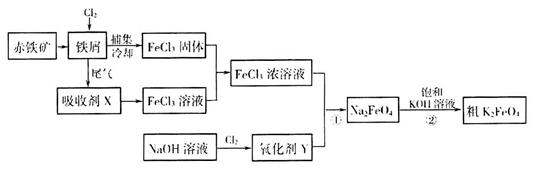
��ش���������
��1����֪����Fe2O3��s��+3C(ʯī) 2Fe(s)+3CO��g����H=+489.0KJ��mol
2Fe(s)+3CO��g����H=+489.0KJ��mol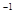 ��
��
��C(ʯī)+CO2��g�� 2CO(g)��H=+172.5KJ��mol
2CO(g)��H=+172.5KJ��mol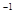 ���ó�����Ϊԭ���ڸ�¯���������з�������Ҫ��ӦΪFe2O3��s��+3CO(g)
���ó�����Ϊԭ���ڸ�¯���������з�������Ҫ��ӦΪFe2O3��s��+3CO(g) 2Fe(s)+3CO2��g����H=??KJ��mol
2Fe(s)+3CO2��g����H=??KJ��mol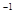 ��
��
��2�����ռ�x������Ϊ____________(д��ѧʽ)��
��3��������YΪ��84����Һ������Ч�ɷ֣����ڼ��������·�Ӧ�ٵ����ӷ���ʽΪ
__________________________________________________________________
��4�����̢�����ij�����½��еģ���Ӧ�Ļ�ѧ����ʽΪ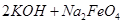 =
=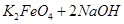 ��˵�����¶���
��˵�����¶���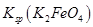 __________
__________ 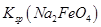 (�>����<��)��
(�>����<��)��
�ٶ��˹�����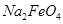 ��ȫת��Ϊ
��ȫת��Ϊ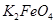 ���������Ƶôֲ�Ʒ
���������Ƶôֲ�Ʒ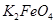 206.25t����Ʒ����Ϊ96������������������Ҫ������Y��������___________t��
206.25t����Ʒ����Ϊ96������������������Ҫ������Y��������___________t��
��5�����������һ�����Ͷ��ε�أ����ҺΪǿ����Һ�����ط�ӦΪ��3Zn+2K2FeO4+8H2O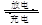 3Zn��OH��2+2Fe��OH��3+4KOH���ŵ�ʱ��صĸ�����ӦʽΪ______________________________________��
3Zn��OH��2+2Fe��OH��3+4KOH���ŵ�ʱ��صĸ�����ӦʽΪ______________________________________��
�ο��𰸣���1����28.5 ��3�֣�??????��2��FeCl2��3��
���������
�����������1����֪����Fe2O3��s��+3C(ʯī) 2Fe(s)+3CO��g����H=+489.0KJ��mol��1��
2Fe(s)+3CO��g����H=+489.0KJ��mol��1��
��C(ʯī)+CO2��g�� �����Ѷȣ���
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ�У���ȷ���ǣ�������
A����ⱥ��ʳ��ˮ��2C1-+2H2O�TH2��+C12��+2OH-
B��̼����ˮ���Լ��ԣ�C
O
2-3
+2H2O?H2CO3+20H-
C����ĩ���ԭ����3HCO
-3
+A13+�TAl��OH��3��+3CO2��
D������FeBr2������ˮ�У�2Fe2++2Br-+2C12�T2Fe3++Br2+4C1-
�ο��𰸣�A�����ʳ��ˮ���缫����δ֪����ʹ�ö��Ե缫ʱ������2C1-
���������
�����Ѷȣ���
3��ѡ���� ��һ����������Ͷ��Ca(HCO3)2��Һ��,�ж����Ӧ����,�����йص����ӷ���ʽ��ȷ����
A��2Na + 2H+ = 2Na+ + H2��
B��Ca2+ + HCO3��+ OH- =CaCO3�� + H2O
C��Ca2+ + 3HCO3��+ 3OH-=CaCO3�� + 2CO32��+ 3H2O
D��Ca2+ + 2HCO3��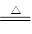 CaCO3�� + CO2�� + H2O
CaCO3�� + CO2�� + H2O
�ο��𰸣�BD
������������ܽ��ڣ�����NaOH���ų�����
A��ˮΪ������ʲ��ܲ�2Na + 2H2O = 2Na+ + 2OH��H2��
C������֮�����Ȳ�������ʵ
�����Ѷȣ�һ��
4��ѡ���� �������ӷ���ʽ�У���ȷ����
A�������Ȼ�����Һ��Ӧ��Fe + Fe3+ ="=" 2Fe2+
B������ʯ��ϡ���ᷴӦ��CO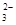 + 2H+ ="=" CO2 �� + H2O
+ 2H+ ="=" CO2 �� + H2O
C��ͭ��ϡ���ᷴӦ��Cu + H+ + NO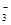 ="=" Cu2+ + NO�� + H2O
="=" Cu2+ + NO�� + H2O
D������������������Һ��Ӧ��Cl2 + 2OH��="=" Cl�� + ClO�� + H2O
�ο��𰸣�D
���������Aѡ���ɲ��غ㣬������ʯ�������ﲻ�ܲ�B����Cѡ���ɲ��غ㣬C�����������������Ƶķ�Ӧ��ȷ�����Դ�ѡD��
�����Ѷȣ���
5��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A����NaAlO2��Һ��ͨ�����CO2��2AlO2�� + CO2 + 3H2O��2Al(OH)3�� + CO32��
B��С�մ�������������Һ��ϣ�HCO3�� + OH����CO2��+H2O
C����̼��������Һ�м������������������Һ��Ba2��+OH��+HCO3���� BaCO3��+H2O
D�����Ȼ�����Һ�ͷ�ˮ��Ӧ��ȡ�����������壺Fe3����3H2O(��ˮ)��Fe(OH)3����3H��
�ο��𰸣�C
���������
���������A�����CO2�����ӦΪHCO3�����ʴ���B�ӦΪHCO3�� + OH����CO32��+H2O���ʴ���D���ӦΪ���淴Ӧ���ʴ�����ѡC��
���������ӷ���ʽ�����ж�Ҫע�⣺��ԭ���Ƿ���Ͽ���ʵ�����Ƿ���������غ㡢���Ƿ���ϵ���غ㡢���Ƿ���ϵ�ʧ������ȡ����ܵ���������ʲ�����ӡ�ע������������������ȡ�
�����Ѷȣ���