微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据下图,可判断出下列离子方程式中错误的是
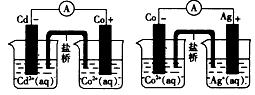 [???? ]
[???? ]
A. 2Ag(s)+Cd2+(aq)=2Ag+(aq)+Cd(s)
B. Co2+(aq)+Cd(s)=Co(s)+Cd2+(aq)
C. 2Ag+(aq)+Cd(s)=2Ag(s)+Cd2+(aq)
D. 2Ag+(aq)+Co(s)=2Ag(s)+Co2+(aq)
参考答案:A
本题解析:
本题难度:简单
2、选择题 某原电池装置如图所示。下列有关叙述中,正确的是(? )
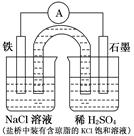
A.Fe作正极,发生氧化反应
B.负极反应:2H++2e-=H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.工作一段时间后,NaCl溶液中c(Cl-)增大
参考答案:D
本题解析:A项,Fe作负极,发生氧化反应,不正确;B项,负极反应为:Fe-2e-=Fe2+,故不正确;C项,因为正极反应为:2H++2e-=H2↑,故右侧烧杯中溶液的pH增大,不正确;D项,因为在原电池盐桥中Cl-离子向负极移动,故NaCl溶液中c(Cl-)增大,正确。
本题难度:一般
3、填空题 (15分)纳米级Cu2 O 粉末,由于量子尺寸效应,其具有特殊的光学、电学及光电化学性质,在太阳电池、传感器、超导体、制氢和电致变色、环境中处理有机污染物等方面有着潜在的应用。
Ⅰ.纳米氧化亚铜的制备
(1)四种制取Cu2O的方法如下:
①火法还原。用炭粉在高温条件下还原CuO;
②最新实验研究用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。
已知:N2H4(l)+O2(g) N2(g)+2H2O(l)???△H="-a" kJ/mol
N2(g)+2H2O(l)???△H="-a" kJ/mol
Cu(OH)2(s) CuO(s)+H2O(l)??△H="b" kJ/mol
CuO(s)+H2O(l)??△H="b" kJ/mol
4CuO(s) 2Cu2O(s)+O2(g)??????△H="c" kJ/mol
2Cu2O(s)+O2(g)??????△H="c" kJ/mol
则该方法制备Cu2O的热化学方程式为?????????????????????????????????????????????。
③工业中主要采用电解法:用铜和钛作电极,电解氯化钠和氢氧化钠的混合溶液,电解总方程式为:2Cu+H2O Cu2O+H2↑,则阳极反应式为:???????????????????????????????。
Cu2O+H2↑,则阳极反应式为:???????????????????????????????。
④还可采用Na2SO3还原CuSO4法:将Na2SO3 和CuSO4加入溶解槽中,制成一定浓度的溶液,通入蒸气加热,于100℃~104℃间反应即可制得。写出该反应的化学方程式:???????????????。
Ⅱ.纳米氧化亚铜的应用
(2)用制得的Cu2O进行催化分解水的实验
①一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入10. 0 mol水蒸气,发生反应:
2H2O(g)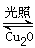 2H2(g)+O2(g)?△H=+484 kJ・mol-1
2H2(g)+O2(g)?△H=+484 kJ・mol-1
T1温度下不同时段产生O2的量见下表:
时间/min
| 20
| 40
| 60
| 80
|
n(O2)/mol
| 1.0
| 1.6
| 2.0
| 2.0
前20 min的反应速率v(H2O)=???????????????????????;该该温度下,反应的平衡常数的表达式K=?????????????;若T2温度下K=0.4,T1?????????T2(填>、<、=)
②右图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为??????,t2时改变的条件可能为??????????????;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为????????????????;

③用以上四种方法制得的Cu2O在其它条件相同下分别对水催化分解,产生氢气的速率v随时间t变化如图所示。下列叙述正确的是??????????。
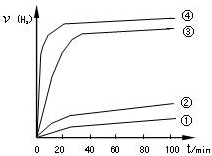
A.方法③、④制得的Cu2O催化效率相对较高
B.方法④制得的Cu2O作催化剂时,水的平衡转化率最高
C.催化效果与Cu2O颗粒的粗细、表面活性等有
D.Cu2O催化水分解时,需要适宜的温度
参考答案:Ⅰ、(1)②4Cu(OH)2(s)+ N2H4(l)
本题解析:Ⅰ、(1)②考查盖斯定律的应用。根据已知反应可知,②×4+③-①即得到4Cu(OH)2(s)+ N2H4(l) 2Cu2O(s)+N2(g)+6H2O(l),所以反应热△H=(4b+c-a)kJ/mo。 2Cu2O(s)+N2(g)+6H2O(l),所以反应热△H=(4b+c-a)kJ/mo。
③电解池中阳极失去电子,所以根据总反应式可知,阳极是铜失去电子,被氧化生成氧化亚铜,方程式为2Cu+2O
本题难度:一般
4、选择题 关于如图装置的叙述中,正确的是
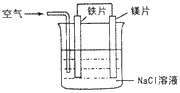 [???? ] [???? ]
A.镁片为负极,镁片上产生黄绿色气体
B.铁片为阳极,铁片上产生无色气体
C.溶液中铁片与镁片之间产生白色沉淀
D.溶液中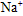 向镁片方向定向移动 向镁片方向定向移动
参考答案:C
本题解析:
本题难度:一般
5、选择题 铜锌原电池(如图)工作时,下列叙述正确的是
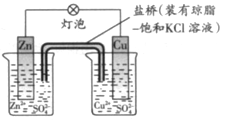
A 正极反应为:Zn―2e-=Zn2+? B电池反应为:Zn+Cu2+=Zn2+ +Cu?
C 在外电路中,电流从负极流向正极?? D 盐桥中的K+移向ZnSO4溶液
参考答案:D
本题解析:略
本题难度:简单
|